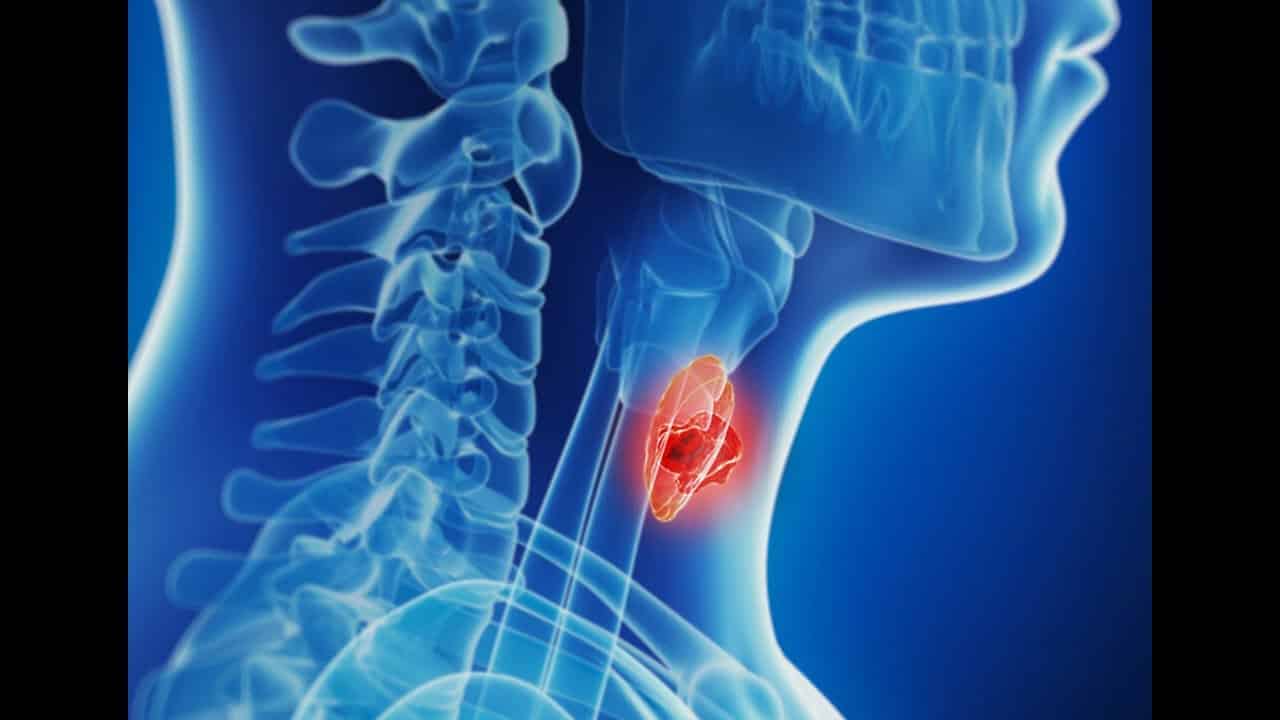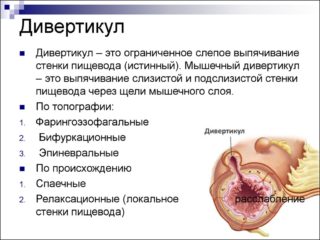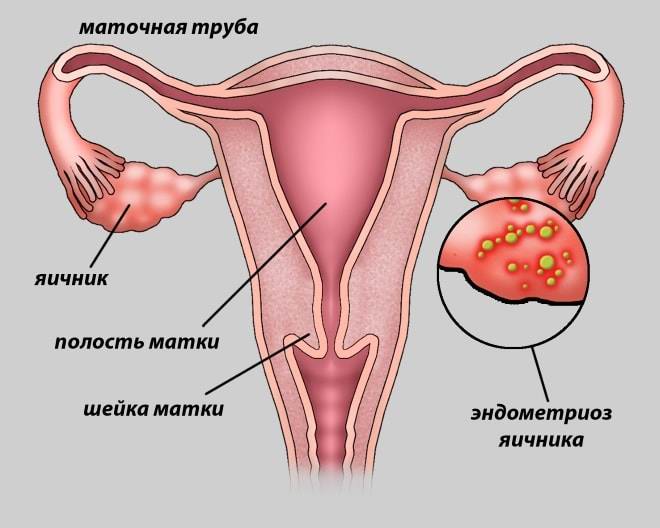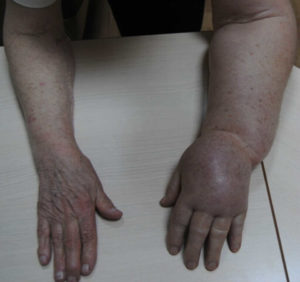
Постмастэктомический синдром: патогенез отека, осложнения, терапевтические меры
Постмастэктомический синдром развивается после операции по удалению молочной железы. Это состояние характеризуется отеками, изменениями кожи, расстройствами различного характера. Лечение постмастэктомического синдрома требует комплексного подхода, предусматривающего применение физиотерапевтических и физических методик, медикаментозных средств.
Особенности постмастэктомического синдрома
В среднем на том, чтобы появились первые признаки данного расстройства, уходит 10-24 месяца после радикальной мастэктомии. В редких случаях симптомы синдрома проявляются спустя 10 и более лет.
По статистике, чаще патологическое состояние развивается после радикальной мастэктомии на правой груди. Без врачебного вмешательства синдром существенно ухудшает качество жизни пациенток и приводит к инвалидности.
Причины
Вероятность проявления постмастэктомического синдрома отчасти зависит от особенностей проведенной операции. Также на это влияет характер течения восстановительных процессов и реабилитации пациентки после хирургического вмешательства. В связи с этим выделяют несколько причин возникновения постмастэктомического синдрома:
- Нарушение микроциркуляции крови. В ходе операции удаляется несколько коллекторов, расположенных возле пораженной груди и отвечающих за отток лимфатической жидкости. Одновременно с этим возможен спазм сосудов из-за механических повреждений. Такое воздействие приводит к воспалению местных тканей и последующим развитием тромбофлебита или лимфангиита.
- Повреждение нервных тканей. Во время радикальной мастэктомии хирург иссекает и удаляет множество волокон, составляющих молочную железу. Из-за повреждения нервов нарушается иннервация плечевого сустава, верхней конечности и шеи. После иссечения пациентки испытывают постоянную боль и жалуются на снижение чувствительности указанных зон. Данное состояние известно как скаленус-синдром.
- Иссечение мышц груди. После удаления этих тканей снижается подвижность плечевого пояса. Данное нарушение диагностируется в 40% случаев.
- Рубцевание тканей. Часто после радикальной мастэктомии (особенно, если операция сопровождается радиотерапией) происходит разрастание фиброзной ткани. Наиболее выражены такие изменения в случаях, когда во время восстановления пациентки произошло инфицирование и нагноение тканей.
Механизм развития
Постмастэктомический синдром развивается в несколько этапов. Сначала в проблемной зоне происходит спазм сосудов из-за накопления тромбоцитов, к чему приводит повреждения местных тканей. Эти нарушения провоцируют нарушение микроциркуляции, что способствует отеканию проблемной зоны.
Ввиду того что после операции снижается подвижность верхней конечности, мышцы руки теряют способность выполнять насосную функцию. Из-за этого вода, белки и соли постепенно накапливаются в зоне поражения, усиливая отечность.
Кроме того, развитию приведенных нарушений способствует разрастание фиброзной ткани, которая сдавливает сосуды.
Градация синдрома
Одна из классификацией построена с учетом выраженности симптоматики:
- 1 степень. Отек локализуется только на пальцах и кисти руки, расположенной со стороны удаленной груди. В проблемной зоне снижается температура тела. Отек занимает не более 25% верхней конечности.
- 2 степень. Отек распространяется на ткани предплечья. Кожа сильно натянутся. Отек захватывает до 50% пораженной конечности. Также отмечается снижение температуры тела в зоне поражения.
- 3 степень. Отек распространяется на плечо и не спадает в течение продолжительного временного отрезка. Кожу невозможно взять в складку. Низкая температура тела и отек отмечаются на 70% поверхности руки.
- 4 степень. Развивается деформация конечности, из-за чего рукой сложно двигать. В зоне поражения появляются трофические язвы. Температура тела снижена на всей поверхности руки, включая плечо.
Помимо указанной классификации в отечественной медицине принято выделять несколько стадий развития постмастэктомического синдрома, каждая из которых характеризуется собственными признаками:
- Доклиническая. На этой стадии не выявляются выраженные изменения в проблемной зоне и верхней конечности. Кожа сохраняет прежнюю эластичность, а поверхность дермы остается гладкой. Пациентка не испытывает дискомфорта как в состоянии покоя, так и при совершении движений.
- Начальная. Данная стадия характеризуется появлением незначительного отека со стороны удаленной железы. Этот симптом беспокоит обычно по вечерам. Объем окружности плеча на начальной стадии немного увеличен. У пациентки возникают периодически боли со стороны поражения. Кожа на данном этапе постепенно меняет окрас и теряет прежнюю эластичность.
- Стадия умеренных ощущений. Этот этап характеризуется постоянным отеком, который захватывает всю конечность вплоть до плеча. Кожа приобретает бледный цвет с синюшным оттенком.
- Стадия выраженных ощущений. Кожа на пораженной конечности приобретает плотную консистенцию. На этой стадии отмечаются признаки деформации тканей, из-за чего снижается подвижность руки. Происходящие изменения провоцируют нарушение чувствительности, частые боли.
Симптомы
О сновным симптомом постмастэктомического синдрома является отечность верхней конечности, которая постепенно нарастает. Данный признак редко возникает сразу после операции по удалению молочной железы. Обычно между мастэктомией и появлением симптомов синдрома проходит несколько месяцев.
сновным симптомом постмастэктомического синдрома является отечность верхней конечности, которая постепенно нарастает. Данный признак редко возникает сразу после операции по удалению молочной железы. Обычно между мастэктомией и появлением симптомов синдрома проходит несколько месяцев.
В первое время отек локализуется на пальцах и кистях, нарушая подвижность последних. Из-за этого пациентка испытывает трудности с надеванием ювелирных украшений. Нередко в области кисти возникает чувство тяжести.
По мере прогрессирования постмастэктомического синдрома отек распространяется выше, захватывая:
- предплечье;
- плечо;
- надплечье;
- ключицу, шею, грудную клетку (встречается редко).
В первое время кожа в проблемной зоне остается неизменной. Но развивающийся патологический процесс провоцирует следующие нарушения:
- сухость;
- шелушение;
- побледнение;
- снижение температуры тела в проблемной зоне на 0,5-1 градус.
В дальнейшем пораженные ткани начинают уплотняться, из-за чего возникают трудности с формированием складки из кожи. В запущенных случаях формируются трофические язвы.
Появление указанных симптомов провоцирует развитие депрессии у пациентки с соответствующими клиническими признаками.
Возможные осложнения
У большинства пациенток развитие постмастэктомического синдрома вызывает следующие осложнения:
- снижение подвижности руки со стороны удаленной молочной железы;
- полинейропатическое расстройство;
- брахиоплексит;
- неспособность полностью сгибать конечность в суставе (контрактура).
В запущенных случаях, когда отек распространяется на большую часть руки, возможно появление рожистого воспаления. Из-за застоя лимфатической жидкости у некоторых пациенток возникает лимфангиосаркома (синдром Стюарта-Тривса).
Методы диагностики
Диагностика постмастэктомического синдрома начинается с осмотра проблемной конечности и оценки характера поражения. В частности, врач определяет площадь распространения отека, степень чувствительности кожи, а также насколько ограничена подвижность руки.
С целью определения запущенности случая (оценки повреждений сосудов) назначаются следующие процедуры:
- Лимфосцинтиграфия. Метод позволяет визуализировать каналы лимфатической системы и выявить зоны застоя и оценить скорость движения жидкости.
- Дуплексное сканирование. Применяется для оценки скорости кровотока, проходимости сосудов.
- Флебография. К этому методу прибегают для проверки состояния подмышечной и подключевой вен. Посредством флебографии выявляется стеноз сосудов и локализация нарушения.
- Электронейромиография. Метод используется для оценки функционального состояния нервных волокон и скорости прохождения (иннервации) импульсов.
Дополнительно назначаются лабораторные анализы, позволяющие оценить функцию кроветворения. В запущенных случаях прибегают к КТ и МРТ, с помощью которых определяют различные нарушения.
Несмотря на том что постмастэктомический синдром отличается характерными симптомами, важно дифференцировать это состояние с опухолями и сосудистыми патологиями.
Лечение
Физиотерапия
Физиотерапия призвана восстановить тонус кровеносных и лимфатических сосудов. Для этого применяются:
- пневматическая компрессия;
- лимфодренаж (ручной либо механический);
- фототерапия;
- гидрокинезотерапия;
- низкочастотная электронейростимуляция мышечных волокон;
- лазеротерапия.
Физиотерапевтические процедуры дополняются ношением специальных бандажей или повязок, ЛФК. Подавить болезненные ощущения помогает воздействие ультразвуком. Этот также позволяет восстановить чувствительность и подвижность конечности.
Медикаментозная терапия
В рамках медикаментозной терапии используют венототики, которые восстанавливают тонус и функции лимфатической системы:
- «Кумарин»;
- «Венастат»;
- «Аэсцин»;
- «Троксевазин» и другие.
При трофических язвах показано применение витамина Е и «Пентоксифиллина». В случае инфицирования открытых ран и развития гнойного процесса рекомендованы антибиотики широкого спектра действия.
Для подавления болевого синдрома назначаются психоаналептики и протеолитические ферменты. При необходимости лекарственную терапию дополняют седативными средствами нестероидными противовоспалительными препаратами.
Хирургическое вмешательство
Хирургическое вмешательство при постмастэктомическом синдроме применяется редко. К этому методу лечения прибегают, когда отек распространяется на большую часть руки, что вызывает соответствующие изменения.
В случае, если снижается чувствительность кожи и подвижность конечности, проводится иссечение и последующий перенос несколько групп мышц. С помощью этой процедуры восстанавливается кровообращение и устраняются указанные нарушения.
При парестезиях показана операция по нормализации нервной проводимости.
Профилактика
Вне зависимости от характера поражения и выбранной тактики лечения пациенткам рекомендуют ношение эластичного бинта или компрессионного белья, с помощью которого снижается интенсивность симптоматики.
Во избежание развития синдрома, а также с целью профилактики обострений, рекомендуется соблюдать следующие правила:
- отказаться от подъема тяжестей;
- ограничит подвижность пораженной конечности;
- избегать травм и перегрева руки;
- регулярно проводить анализ крови и контролировать артериальное давление;
- носить свободную одежду;
- надевать перчатки при выполнении работ по дому с целью профилактики заражения;
- выполнять лечебные упражнения;
- употреблять больше жидкости при авиаперелетах;
- контролировать вес;
- отказаться от алкоголя и курения.
Прогноз
 Несмотря на то что постмастэктомический синдром плохо поддается коррекции, при своевременном врачебном вмешательстве и правильно подобранной схеме терапии удается значительно снизить отек и интенсивность болезненных ощущений. Начиная с третьей недели после операции по поводу злокачественной опухоли рекомендуется самостоятельно массировать мышцы руки, расположенной со стороны удаленной молочной железы. Это поможет предупредить развитие постмастэктомического синдрома. Впоследствии необходимо уменьшить уровень физической нагрузки на проблемную конечность.
Несмотря на то что постмастэктомический синдром плохо поддается коррекции, при своевременном врачебном вмешательстве и правильно подобранной схеме терапии удается значительно снизить отек и интенсивность болезненных ощущений. Начиная с третьей недели после операции по поводу злокачественной опухоли рекомендуется самостоятельно массировать мышцы руки, расположенной со стороны удаленной молочной железы. Это поможет предупредить развитие постмастэктомического синдрома. Впоследствии необходимо уменьшить уровень физической нагрузки на проблемную конечность.
Постмастэктомический синдром — это целый комплекс разнообразных симптомов, возникающих после удаления молочной железы. Данное состояние характеризуется отеком руки и болевыми ощущениями. Со временем снижается подвижность пораженной конечности, что может привести к инвалидности.
Постхолецистэктомический синдром

Общие сведения
Постхолецистэктомический синдром (ПХЭС) – это целый комплекс симптомов, которые проявляются у человека после того, как ему провели удаление желчного пузыря. Для этого состояния характерны приступы боли, проблемы с пищеварением, диарея, понижение массы тела и др.
Согласно медицинской статистике, постхолецистэктомический синдром, код по МКБ-10 которого — K91.5, проявляется у 5–40% пациентов. Специалисты предполагают, что такое состояние является либо продолжением болезни, которая и привела к оперативному вмешательству, либо следствием операции. Как правило, удаление желчного пузыря не приводит к серьезным негативным последствиям для работы желчных путей. Около 10% случаев желчной колики являются следствием нарушений сфинктера Одди – как структурных, так и функциональных. Термин «дисфункция сфинктера Одди» также применяется вместо определения «постхолецистэктомический синдром».
О том, как может проявляться постхолецистэктомический синдром, когда происходит спазм сфинктера Одди и как правильно действовать, чтобы устранить неприятные признаки, речь пойдет в этой статье, где описаны симптомы и лечение постхолецистэктомического синдрома.
Патогенез
У основной части больных с этим синдромом отмечаются функциональные моторные расстройства. Неотъемлемая часть патогенеза желчекаменной болезни – моторные нарушения желчного пузыря и сфинктерного аппарата желчевыводящих путей.
Вследствие удаления желчного пузыря отмечается нарушение функции сфинктерного аппарата желчных путей. Развитие боли после операции, как правило, связано с увеличением давления в билиарном тракте, что связано с нарушениями функции сфинктера Одди.
В организме сфинктер Одди обеспечивает анатомическую и физиологическую связь между желчевыводящими путями, поджелудочной железой и двенадцатиперстной кишкой.
Физиологический контроль сфинктера Одди определяется рядом гормональных и нервных стимулов. В частности, важная роль в этой регуляции отводится гастроинтестинальным гормонам. Особое значение имеет холецистокинин (панкреозимин) и секретин.
Когда желчный пузырь сокращается и синхронно расслабляется сфинктер Одди, концентрированная желчь поступает в двенадцатиперстную кишку. В это время происходит выделение панкреатического сока под действием холецистокинина, что обеспечиваются все условия для расщепления пищи. Если происходит спазм сфинктера этот процесс нарушается.
Желчный пузырь непосредственно задействован в модуляции ответа сфинктера Одди на влияние гастроинтестинальных гормонов. После удаления желчного пузыря реакция сфинктера Одди в ответ на холецистокинин снижается.
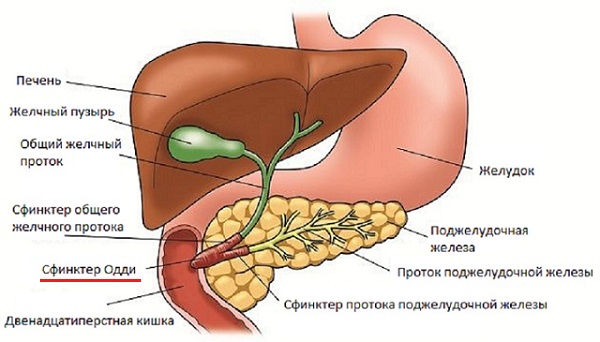
О том, как изменяется функциональное состояние сфинктера Одди после холецистэктомии, существуют разные мнения. В частности, есть теория, что после операции повышается тонус и расширяется общий желчный проток. Также есть мнение, что вследствие холецистэктомии проявляется недостаточность сфинктера Одди, так как он не может длительнее время выдерживать высокое давление желчи. Противоречия, которые отмечаются в описании состояния сфинктера Одди, связаны с тем, что его функции исследовались в разные сроки после проведения холецистэктомии.
Классификация
В современной медицине отсутствует общепринятая классификация постхолецистэктомического синдрома. В зависимости от причины, по которой проявляются такие симптомы, в своей практике медики определяют это состояние широко, применяя такую классификацию:
- Рецидивы образования камней общего желчного протока – как ложные, так и истинные.
- Стенозирующий дуоденальный папиллит.
- Стриктуры общего желчного протока.
- Ограниченный перитонит в хронической форме.
- Холепанкреатит.
- Вторичные гастродуоденальные язвы — билиарные или гепатогенные.
Однако Римские критерии II 1999 года, а также Римские критерии III 2006 года ограничивают рамки «ПХЭС» дисфункцией сфинктера Одди, возникшей после холециетэктомии. Применяется следующая классификация дисфункции сфинктера Одди:
Дисфункция сфинктера Одди по билиарному типу. Определяется три типа этой разновидности:
- Билиарный тип I – проявляются типичные приступы боли продолжительностью 20 и больше минут; общий желчный проток расширяется больше, чем на 12 мм; при проведении эндоскопической ретроградной панкреатохолангиографии выведение контрастного вещества замедляется больше, чем на 45 минут; отмечается превышение нормы трансаминаз и/или щелочной фосфатазы.
- Билиарный тип II – проявляются приступы болей билиарного типа; до 63% пациентов имеют манометрическое подтверждение сфинктера Одди. При этом возможны и структурные, и функциональные нарушения.
- Билиарный тип III – проявляются приступы болей билиарного типа без объективных нарушений. Манометрическое подтверждение сфинктера Одди отмечается только у 12-28% пациентов. Как правило, дисфункция имеет функциональную природу.
Дисфункция сфинктера Одди по панкреатическому типу. Панкреатический тип проявляется эпигастральной болью, которая характерна для панкреатита. Боль отдает в спину и уменьшается, когда пациент наклоняется вперед. У больного значительно повышается сывороточная амилаза и липаза. При манометрии определяется дисфункция сфинктера Одди в 39–90% случаях.
Дисфункция сфинктера Одди по смешанному типу. Смешанный тип характеризуется опоясывающей болью, или боль локализуется в эпигастрии. Также проявляются другие признаки, характерные как для билиарного, так и для панкреатического типов.
Причины
Чаще всего признаки ПХЭС проявляются вследствие таких причин:
- Камни в желчевыводящих протоках (холедохолитиаз). Это могут быть как рецидивы желчнокаменной болезни, когда происходит повторное образование камней, так и ложные рецидивы с оставшимися конкрементами. В большинстве случаев остаются именно те камни, которые не были удалены во время первой операции.
- Органические и функциональные изменения большого дуоденального сосочка (БДС). Эта причина приводит к появлению болей, температуры и желтухи после удаления желчного пузыря. После такого вмешательства у большинства больных на некоторое время усиливается тонус сфинктера БДС. Но при отсутствии патологических изменений тонус постепенно приходит в норму. Примерно у четверти прооперированных людей отмечается стеноз БДС. Сначала развивается отек, после чего, при продолжительной травматизации при прохождении камней, отмечается его сужение.
- Повреждения желчных протоков и стриктуры. Сужение протока происходит или вследствие изменений стенки, связанных с воспалением, или является следствием нахождения там камня. Иногда на это влияют внешние причины.
- Холангит. При плохом высвобождении желчиона застаивается в желчевыводящих путях. Как следствие, создаются условия для восходящего распространения инфекции. При холецистэктомии происходит удаление только одного очага инфекции, но протоки могут остаться инфицированными.
- Особенности проведения операции. Рецидив болей развивается в том случае, если в оставленной части желчного пузыря или культе содержатся камни или сгущенная желчь.
- Опухоли желчных протоков. Их могут не обнаружить в процессе операции или они появляются позже.
- Болезни двенадцатиперстной кишки. У людей с болезнями желчевыводящих путей часто отмечаются отек и гиперемия слизистой оболочки двенадцатиперстной кишки, ее атрофия, нарушения моторной функции.
- Панкреатит в хронической форме. Часто встречается у людей, которые перенесли холецистэктомию. При технически правильно проведенной холецистэктомии отток панкреатического сока улучается и восстанавливается внешнесекреторная функция железы. Но если фиброзные изменения ярко выражены, то после операции панкреатит может проявиться как самостоятельная болезнь.
- Другие причины. Рецидив болей после проведенной операции могут спровоцировать дисбактериоз, колит, нарушение кишечного всасывания, гемолитическая болезнь, а также заболевания почек, толстой кишки, позвоночника. Боли, не связанные с изменениями желчевыводящей системы, тоже могут восприниматься как ПХЭС.
Симптомы постхолецистэктомического синдрома
Основные симптомы спазма сфинктера Одди – это проявление приступов сильных или средней интенсивности болей, которые продолжаются более 20 минут и проявляются на протяжении больше чем трех месяцев. Также проявляются диспепсические и невротические расстройства. Беспокоит тяжесть в правом подреберье. Как правило, боль постоянная. Иногда приступы сначала проявляются редко и длятся несколько часов, а потом, в промежутках между приступами, боль вообще не ощущается. У некоторых больных со временем частота приступов и интенсивность болей увеличивается. Связь приступов с приемом пищи у всех проявляется по-разному. Но наиболее часто боль беспокоит через 2-3 часа после еды.
Иногда, в тяжелых случаях, боль длительна и упорна, она сочетается со рвотой и тошнотой, а также с мучительными приступами изжоги.
Если причины ПХЭС связаны с истинным рецидивом образования камней желчного протока, то неприятные симптомы появляются не раньше, чем через несколько лет после проведенной операции. В таком случае развиваются следующие признаки:
- Боль в правом подреберье и в правой части эпигастральной области — как правило, монотонная, реже в виде приступов. В большинстве случаев боль менее сильная, чем до проведения операции.
- Нарушения циркуляции желчи, что подтверждает диагностика.
- Инфекционно-воспалительный процесс, который развивается вследствие нарушения циркуляции желчи. Он проявляется лихорадкой, плохим самочувствием. У больного повышается СОЭ. Если развивается гнойный холангит, симптомы усугубляются.
- При ложном рецидиве камнеобразования желчного протока проявления аналогичны истинному рецидиву. Но при таком состоянии симптомы появляются раньше — примерно через 2 года после операции.
Анализы и диагностика
 Люди, которым была проведена холецистэктомия, находятся на диспансерном наблюдении у специалиста с целью раннего определения неблагоприятных результатов, а также обеспечения важных профилактических мероприятий и контроля выполнения рекомендаций пациентом.
Люди, которым была проведена холецистэктомия, находятся на диспансерном наблюдении у специалиста с целью раннего определения неблагоприятных результатов, а также обеспечения важных профилактических мероприятий и контроля выполнения рекомендаций пациентом.
В процессе диагностики проводится ряд исследований и лабораторных анализов. Врач обязательно изучает анамнез, проводит опрос и осмотр пациента. Для установления диагноза проводят:
- Общий анализ крови.
- Биохимический анализ крови, в процессе которого определяются биохимические маркеры синдрома холестаза-цитолиза.
- Анализ мочи.
- Электрокардиография.
- Рентгеноскопия грудной клетки.
- Ультразвуковое исследование.
- ФГДС.
- КТ, МРТ.
В процессе обследования больных, которые жалуются на признаки ПХЭС, используется принцип поиска причин таких проявлений от более простых к сложным, а также использования методик от неинвазивных к более травматичным, но позволяющим получить важную информацию.
Еще один важный момент касается хирургической настороженности при таких симптомах: она должна быть тем больше, чем меньше времени прошло от операции.
Как правило, после лабораторных анализов обследование таких больных начинают с проведения УЗИ брюшной полости, которое дает возможность исключить анатомические изменения органов и перейти к более целенаправленным обследованиям.
Однако, несмотря на то, что возможности современной диагностики достаточно широкие, у определенного количества людей не удается выяснить причину неприятных симптомов после перенесенной холецистэктомии.
Лечение постхолецистэктомического синдрома
Очень важно, чтобы лечение постхолецистэктомического синдрома было комплексным и направлялось на устранение причин проявления неприятных симптомов. Пациенту, который перенес удаление желчного пузыря, необходимо помнить, что правильное питание, четкий режим приема пищи, физическая активность – это важнейшие условия успешной реабилитации после хирургической операции. Также при проявлении болей и других неприятных симптомов проводится медикаментозное лечение.
Как бороться с постмастэктомическим синдромом
Когда дело касается полноценной жизни женщины после мастэктомии, тут не всё так однозначно. Удаление молочной железы – чрезвычайно травматическая процедура. Вместе с поражённым органом удаляются окружающие его ткани. Это грудная мышца, сосудистый пучок, и, что самое важное, подмышечные лимфоузлы с её сосудами, по которым ранее свободно циркулировала лимфа, обеспечивающая нормальную работу иммунной системы. И вот целого пласта этой системы в организме не стало. Возникает так называемый постмастэктомический синдром.

«Тяжёлая рука»
Раковые опухоли имеют мерзкое свойство осуществлять инфильтрацию своих клеток по току крови. Этот процесс называется метастазированием, а такие клетки – метастазами. Укоренившись, задержавшись в любом органе, куда её занесёт кровь или лимфа, такая клетка сохраняет способность делиться дальше, вовлекая в онкологический процесс другие органы.
Метастазирование обычно начинается на III стадии рака. Но иногда уже на II. Поэтому, чтобы исключить этот процесс, хирурги удаляют не только саму опухоль, но и близлежащие ткани.
В случае рака молочной железы это:
- Сама молочная железа – даже если размер опухоли не превышал 3-4 см.
- Грудная мышца под молочной железой.
- Сосудистые пучки.
- Часть подмышечной лимфосистемы, куда, вероятнее всего, могли попасть метастазы по току лимфы.
Это и есть мастэктомия. Операция крайне травмирующая, особенно с применением методик по Холстеду-Майеру (самый травматичный метод мастэктомии, применяемый, когда остальные методы бессильны, есть риск сохранения возникших метастазов), Пирогову и Маддену, а также при двусторонней мастэктомии, т.н. билатеральной.
В большинстве случаев, когда стадия рака более II, хирургическому вмешательству предшествует химиотерапия, а после операции – лучевая, которая добавляет деформации в уже прооперированную ткань в виде лучевого ожога.
Особо нужно остановиться на рубцах после удаления подмышечных лимфоузлов.
Как проявляется постмастэктомический синдром
Клиника проявлений мастэктомического синдрома после удаления подмышечных лимфоузлов носит функциональный и органический характер.
Это проявляется в:
- Нарушении оттока лимфы, что вызывает отёк руки, соседствующей с прооперированной подмышечной впадиной.
- Нарушении венозного оттока от той же руки, которое выражается в неизбежных стенозах и окклюзиях (частичных или полных непрохождениях) подключичных вен.
- Грубых рубцах — послелучевые, послеоперационные фиброзные деформации мышц и соединительной ткани, а также сосудов.
- В нейропатиях или брахиоплексите – поражении плечевого нервного сплетения.
Эти виды возникших органических поражений характерны для самой травматичной операции по методу Холстеда-Майера (назван по именам внедривших её в хирургическую практику онкологических больных врачей).

Проблемы с дыханием
«А при чём тут это?» – спросит непосвящённый. Большие и малые грудные мышцы являются вспомогательной дыхательной мускулатурой, чем более радикальной была операция, чем больше, по мнению оперирующего врача, была вероятность оседания метастазирующих клеток в этих мышцах, тем меньше мышечной ткани оставалось на их месте.
Следствием такого удаления будет не только затруднённое дыхание, особенно при повышенной мышечной активности, но и нарушение «центровки» тела, или его биомеханического равновесия: ведь суммарный вес удалённых органов в виде мышц, самой молочной железы, соединительной ткани, кожи, удалённых лимфоузлов и сосудов мог достигать 2-3 килограммов!
Все эти факторы, накладываясь друг на друга, формируют подавленное психоэмоциональное состояние, которое тоже, наряду с чисто физическими неудобствами, входит в понятие ПМЭС – постмастэктомического синдрома.
Получается, что это не только комплекс симптомов, проявляющихся непосредственно от нарушения состояния и функционирования органов зоны, подвергшейся операции. Это психологический и соматический негатив, способный ввергнуть женщину не просто в чувство неловкости от своего положения, но и в глубочайшую депрессию от чувства кажущейся неполноценности из-за такого косметического дефекта, как отсутствие груди и уродующих кожу шрамов на месте её удаления.
Сказывается и чисто физическое неудобство от жёсткости рубцов, усугублённых лучевым ожогом, от чувства стягивания кожи и уже упомянутого затруднённого полноценного дыхания. Из-за чувства потери женственности, ощущения уродства резко тормозится либидо, пропадает гармония во внутрисемейных отношениях.
Варианты ПМЭС
В первую очередь, от чего страдают онкологические больные, перенесшие мастэктомию – это отёки мягких тканей руки, прилегающих к операционному полю.
Послеоперационные рубцы радикальнейшим образом меняют привычное состояние органов верхней части грудной клетки в области грудных мышц, подмышки и лопатки со стороны, подвергшейся операции. Особенно тяжело больным, у которых мастэктомия была двусторонней, с удалением обеих молочных желез.
К стягивающему эффекту шрамов и рубцов добавляются также уменьшение эластичности тканей вследствие проведённой химиотерапии. Происходит даже образование своеобразного «панциря» из обожжённых радиацией клеток на внутренних стенках сосудов и в подкожной соединительной ткани – что отнюдь не способствует большей гибкости конечности и всего грудного отдела.
Все эти факторы способны подавлять микроциркуляцию в сосудах руки/рук, плеч, головного мозга, потому что часто пережимаются или частично атрофируются ведущие к нему и от него артерии, вены и лимфососуды.
Такое положение вещей плохо влияет на кровоснабжение органов, не способствует своевременному оттоку лимфы.
Длящийся продолжительное время спазм сосудов, развивающийся на его фоне тромбофлебит и воспаление лимфатических путей вызывают неизбежные при такой клинической картине отёки и рубцы ткани под мышкой. Как следствие – ограниченное движение плеча, нарушение иннервации тканей в прилежащей области.

Соматические проблемы
В комплексе же всё перечисленное вызывает у пациента психологические и соматические проблемы, которые, собственно, и называются ПМЭС, и включают в себя:
- Блокировку путей инфильтрации лимфы от конечности со стороны операции.
- Косметический дефект области груди.
- Существенное уменьшение подвижности конечности в плечевом суставе ( в критических его значениях – даже невозможность поднять руку выше уровня плеча).
- Потеря чувствительности руки, переднего отдела грудной клетки на месте швов и рубцов.
- Депрессия от чувства ложной неполноценности.
Диагностика
Развитие постмастэктомического синдрома после операции удаления опухоли и связанных с нею поражённых тканей неизбежен на 100%. Значит, врачам нужно помочь ей выйти из такого состояния, используя те или иные методы, от медикаментозных до психолого-психиатрической помощи.
Но для точной оценки состояния больной нужно провести ещё правильную диагностику. Для этого оценивают объёмы больной и здоровой руки, замеряя её окружность над локтевым суставом, где отёки обычно выражены ярче всего, замеряют температуру кожи (оценивая, в первую очередь, её неизбежное в таких случаях снижение), оценивают амплитуду и саму возможность движения плечевого сустава, проверяют чувствительность кожи на всём протяжении руки от плеча до запястья.
Благодаря этим манипуляциям оценивается уровень повреждений сосудов, их состояние и функциональность тканей руки.
Дуплексное сканирование
Допплерографическое и ультразвуковое исследования объединяют в методе, называемом дуплексное сканирование. Не инвазивной природы, безопасное и информативное воздействие на организм. По степени достоверности превосходит такой способ получения данных, как флебография, но является более точным и безопасным – особенно в плане ненарушения целостности вен.
Дуплексным сканированием определяют скорость кровотока, отсутствие барьеров в венах и артериях, а также анатомические особенности костной и мышечной тканей.
Лимфосцинтиграфия
Метод радиоизотопного исследования, которым заменили устаревшую лимфографию. Показывает строение лимфосистемы, визуализируя её. Показывает участки, на которых лимфа тормозится, застаивается, вплоть до замера движения лимфы в мм/см в секунду.
Электронейромиография
С применением этой методики можно в физических единицах оценить и построить наглядный график состояния периферической нервной системы в поражённой конечности.
Ко всему этому проводят также традиционные лабораторные исследования крови, и, при необходимости или для уточнения данных – компьютерную или магниторезонансную томографию. Диагностика нарушений функций верхней конечности обычно не представляет труда, после операций картина во многих случаев типична.
Один из самых простых способов узнать степень отёчности и возможности возврата тканей к норме – простое надавливание пальцем на отёкшую ткань и замер времени, которое требуется коже принять своё нормальное состояние, с заравниванием ямки от надавливания.

Ограничения после мастэктомии
Существует инструкция, разработанная обществом National Lymphedema Network для больных, перенесших мастэктомию.
- При появлении хотя бы незначительного отёка любого места на руке со стороны операции немедленно консультируйтесь с врачом.
- При необходимости взятия крови для анализа ни в коем случае не делайте это на руке со стороны, подвергшейся операции. Прооперированы были обе стороны? Тогда пусть кровь возьмут из вены на ноге – и инъекцию сделают туда же!
- Измерять АД следует только на неповреждённой руке.
- В гигиенических процедурах используйте увлажняющие бесспиртовые растворы, насухо, но очень бережно удаляйте мягкими салфетками все следы влаги из складок и межпальцевых промежутков.
- Избегать циклических, повторяющихся движений, с энергичными повторяющимися толканиями или притягивании чего-либо.
- Не переносите тяжести больной рукой. Не носите тяжести на ремне со стороны больного плеча.
- Откажитесь от сдавливающих, стягивающих украшений на больной руке.
- Забудьте о саунах, парных, горячих ваннах. Берегите также больную конечность от воздействия ультрафиолета.
- Берегите руку от инфекции, которую могут вызвать порезы, удары с ушибами, ожоги, укусы или царапины животных.
- При маникюре в салоне предупреждайте специалиста, делающего маникюр, о недопустимости срезания кутикул.
- При перелётах на самолётах, с их неизбежным падением давления в окружающей среде, обязательно используйте накачиваемый пневматический компрессионный рукав.
- Если удалённая грудная железа была более 4-го номера, носить облегчённый протез. Бюстгальтер должен быть бескаркасным, без поддерживающих проволочек и косточек.
- Для удаления волос в области подмышечной впадины использовать только электробритву.
- Не оставляйте без внимания внезапные изменения в состоянии конечности, такие, как сыпь, покраснения кожи на обширных участках, повышение температуры руки. В таких случаях визит к врачу нужно делать немедленно, это симптомы ухудшения или начала лимфедемы.
- Следите за своим весом, своевременно реагируйте на его увеличение. Показаны бессолевая диета, употребление легко усваиваемого белка (рыба, птица, телятина).
Как бороться с постмастэктомическими отёками
Лимфатический дренаж – механический и ручной. Компрессия с использованием пневматического(надувного) рукава, который воздействует на руку от запястья до подмышечной впадины.
Пневматический массаж с физическими упражнениями, дополняющими такой массаж, ношение перчаток из гипоаллергенного эластика.
Лекарственное воздействие
В него входит весь комплекс показанных при ПМЭС медикаментов: комбинации кумарина, троксерутин, веностат. Стойкого восстановительного эффекта можно также добиться сочетанием применения простой смеси растворов новокаина и димексида в виде накожных аппликаций.
Очень помогают антиэндоматозные, вазоактивный, противовоспалительные бензопироны в сочетании с усиливающими их воздействие капилляростабилизаторы, ангиопротекторы и комплексные витамины с выраженным антиоксидантным действием.
Для уменьшения сопутствующим послеоперационному состоянию болей показано также применение протеолитических энзимов и психоаналептиков.
Хирургическое воздействие
Проводится с целью пластики, которая придаёт женщине уверенность в собственной привлекательности, так и для удаления затвердевших в результате лучевого воздействия крупных рубцов.
Применяется редко – в силу неизбежного адреналинового выброса уже однажды травмированного хирургией организма
Лазеро- и фототерапия
При отёках руки в любой её части, от дистальных да проксимальных отделов, можно воздействовать как некогерентным излучением светодиодных ламп с максимальной длиной волны 660 нм (матричная светодиодная установка «Терафот»), так и когерентным (лазерным), низкой интенсивности и постоянного импульса, с длиной волны 632 нм.
Возникновению отёков после мастэктомии способствуют:
- Остеохондроз верхних позвоночных отделов.
- Воспаление локтевых, плечевых суставов.
- Травмы мягких тканей верхних конечностей с рубцовыми образованиями.
Во время онкологии:
- Большие размеры опухолей.
- Обширные метастазы в подмышечных лимфоузлах.
- Существующий на момент болезни или бывший ранее тромбофлебит или флеботромбоз.
- Ударное повреждение мышц.

Возможные осложнения
Постмастэктомический синдром может спровоцировать воспаление сухожилий и окружающей их оболочки на конечности, близкой к операционному полю, воспаление слизистых сумок суставов (бурсит). При бурсите в почти 40% случаев движения рукой во всех направлениях ограничены болевым синдромом, с формированием устойчивой контрактуры.
Может также сформироваться брахиоплексит – поражение плечевого нервного сплетения, способное привести в полной неработоспособности руки, когда малейшее движение вызывает боль в области ключицы.
При выраженных отёках (когда диагностируют III-IV степени), возможны рожистые воспаления тканей.
Крайним следствием отёком при ПМЭС бывает лимфангиосаркома, или синдром Стюарта-Тривса.
Постмастэктомический синдром приводит к резкому понижению самооценки и, как следствие этого, депрессивным синдромам и невротической симптоматике.
Прогноз и профилактика
Не всё так фатально, как кажется. Главное – вовремя среагировать на все этапы развития постмастэктомического синдрома, провести комплекс физиотерапевтических и медикаментозных мероприятий и дать женщине психологическую поддержку как со стороны врачей, так (что ещё более важно) членов её семьи.
После семи послеоперационных дней можно уже делать упражнения для разработки плеча, а после трёх недель после операции начинать активный самомассаж кожи и мускулатуры руки.
В дальнейшем исключать ситуации, когда рука может быть сдавлена или травмирована.
Заключение
О полном выздоровлении после такой травмирующей операции, как мастэктомия, говорить не приходится. Но свести к минимуму последствия, применить самые передовые достижения медицины, а главное, оказать своевременную психологическую помощь – можно вполне.
Бережное отношение к верхним конечностям, вынужденных соседствовать с очагом недавнего заболевания, развивающие, поддерживающие тонус мышц упражнения будут залогом активной и долгой жизни ещё много лет после столь радикальной операции.
Постмастэктомический синдром: помочь пациенту вернуться к полноценной жизни
В структуре заболеваемости злокачественными новообразованиями у женщин рак молочной железы занимает одно из первых мест. Радикальные хирургические вмешательства, лучевая и лекарственная терапия, применяемые при лечении, нередко приводят к серьезным соматическим и психологическим нарушениям, которые трактуются в современной медицине как постмастэктомический синдром, когда у 35—40% пролеченных женщин развивается лимфостаз верхней конечности, у 1,2—11% — плечевые плекситы и нейропатии, у 39,7% — ограничение амплитуды движения в плечевом суставе, а у 25% женщин наблюдается тяжелая психологическая депрессия. Описанный симптомокомплекс приводит к инвалидизации больных, в связи с чем вопросы комплексной реабилитации женщин после мастэктомии представляют большую важность для онкологов, занимающихся этой проблемой. Об инновационных методиках лечения больных с постмастэктомическим синдромом мы побеседовали со специалистами в этой области.
— Михаил Рудольфович, первый вопрос будет к вам. Расскажите, что особенного было разработано на базе вашей клиники для лечения больных с постмастэктомическим синдромом?
М.К.: В нашей клинике разрабатываются инновационные направления лечения, выполняются уникальные хирургические вмешательства с использованием эндохирургической и лазерной техники. Проводится комбинированное лечение с использованием химиолучевого метода, фотодинамической терапии. Впервые в нашей стране разрабатываются детали концепции сторожевых лимфатических узлов в онкологии и исследуются новые технологии поиска микрометастазов. Разрабатываются инновационные направления в лечении больных с опухолями кожи при помощи лазерных технологий. К примеру, в онкологической клинике создан аппарат неинвазивного лазерно-флуоресцентного метода диагностики опухолей кожи. Данная методика позволяет определять степень местного распространения опухолевого процесса, а также диагностировать наличие последнего на самых ранних стадиях заболевания. Разработаны и внедрены в практику новые методы формирования межкишечных анастомозов, что значительно сократило процент их несостоятельности, особенно у больных онкопроктологического профиля. Также был разработан и внедрен для клинического использования комплекс мер по диагностике, лечению и профилактике одного из самых частых осложнений у больных, получавших лечение по поводу рака молочной железы, — постмастэктомического отека верхней конечности — с применением гелий-неонового лазера и метода дозированной компрессии.
— В таком случае, что представляет собой этот синдром? Расскажите о его основных проявлениях у больных.
Л.В.: Нами установлено, что у всех без исключения больных, перенесших радикальное лечение по поводу рака молочной железы, неизбежно формируется постмастэктомический синдром. В основе синдрома лежат множественные и разнообразные сосудисто-неврологические нарушения, сопровождающиеся патологическими изменениями свертывающей системы и реологических свойств крови. Постмастэктомический отек мягких тканей верхней конечности на стороне проведенного по поводу рака молочной железы радикального лечения диагностируется у всех без исключения больных. Даже при “нулевой” степени отека, который не обнаруживается клиническими методами, он легко устанавливается в процессе капилляроскопии по характерным патологическим изменениям. Лимфостаз мягких тканей верхней конечности по-прежнему остается наиболее частым патологическим процессом у больных, перенесших радикальное лечение по поводу рака молочной железы. Важно отметить недостаточную эффективность традиционно применяемых методов как терапевтического, так и хирургического лечения при постмастэктомическом синдроме. Больных с таким синдромом в масштабах планеты около 1 млн человек. Эти пациенты были успешно пролечены по поводу рака молочной железы, но, к сожалению, они так и не смогут быть признаны здоровыми людьми. Прогрессивное развитие лимфедемы конечности, утрата многих мануальных навыков и низкая терапевтическая эффективность проведения общепризнанной восстановительной терапии у больных обуславливают развитие скаленус-синдрома, при котором сдавливаются нервы и сосуды, питающие не только руку, но и плечо, и головной мозг. При обследовании, спустя год и более после радикального лечения по поводу рака молочной железы, скаленус-синдром выявляется у 99,4% больных.
Нами разработан целый комплекс терапевтических мероприятий, улучшающих лечебные результаты. Комплекс предусматривает проведение лазеро- и фототерапии, противоотечного лечения (компрессионная, лекарственная терапия, лечебная физкультура, массаж и т.д.), консервативной релаксации передней лестничной мышцы, а также оказания психолого-психиатрической помощи. Безусловно, выбор тех или иных методов обусловлен прежде всего онкологическим статусом пациента, выраженностью лимфедемы, наличием прочих конкретных нарушений и расстройств, общим состоянием, методами радикального лечения и длительностью времени, прошедшего после его окончания, а также наличием и степенью выраженности сопутствующих заболеваний.
— Можно ли более подробно остановиться на истории вопроса? Как начали разрабатывать комплекс этих мероприятий?
Л.В.: Что касается истории вопроса в рамках нашей клиники, то в 1977 году мой учитель, в то время заведующий кафедрой онкологии ММСИ, профессор В.И. Пронин предложил мне, выпускнику лечебного факультета, более детально заняться изучением проблемы реабилитации больных после мастэктомии. Именно тогда мы определили само понятие постмастэктомического синдрома (до этого использовался термин “постмастэктомический отек”), разработали первые отечественные текстильные компрессионные изделия, на которые получили авторские свидетельства. Вообще, стали серьезно разрабатывать методы улучшения качества жизни больных после радикальной операции по поводу рака молочной железы. Ведь когда удаляют молочную железу с регионарным лимфатическим аппаратом, то идет активное накопление лимфы в тканях конечности. Мы разработали специальную саморазжимающуюся гофрированную емкость, обеспечивающую активный дренаж лимфы из послеоперационной раны, специальные компрессионные повязки. Все эти нововведения позволили снизить уровень лимфореи, ускорили процесс заживления и дали возможность начинать реабилитационные мероприятия (противоотечную терапию, лечебную физкультуру) у больных уже в раннем послеоперационном периоде. Впоследствии на нашей кафедре по различным аспектам данной проблемы было защищено несколько докторских и кандидатских диссертаций. Ряд из них был отмечен государственными премиями.
В результате на базе нашей кафедры в центре ОАО “РЖД” был создан уникальный лечебный комплекс, который призван помочь больному вернуться к полноценной жизни, восстановить тонкие мануальные навыки, позволить забыть об инвалидности.
— Расскажите более подробно о восстановительном лечении больных с постмастэктомическим синдромом.
М.С.: Лечение больных раком молочной железы неизбежно сопровождается повышенным травматизмом. Помимо оперативного вмешательства во всем мире применяется медикаментозная и лучевая терапия, наносящая весьма сильные повреждения не только здоровым тканям, но и всему организму в целом. В результате у пациентов развивается целый комплекс различных нарушений, который на сегодняшний день мы называем постмастэктомическим синдромом. Это не только отек верхней конечности, но и постоперационный и постлучевой фиброз мягких тканей, развитие нарушений мозгового кровообращения, повреждение периферических нервов и др. В результате больные становятся тяжелыми инвалидами, причем зачастую без надежды на то, что они когда-нибудь избавятся от этой патологии. Казалось бы, эти больные победили, избавились от такого тяжелого, смертельного заболевания, перенесли сложную операцию и не менее тяжелое и травматичное лучевое лечение, а стали инвалидами. Традиционно все специалисты (физиотерапевты, массажисты), которые занимаются реабилитацией пациентов, очень настороженно относятся к лечению онкологических больных и, к сожалению, нередко отказывают им в помощи. В нашей клинике нашли решение этой проблемы. Мы осуществляем комплексную терапию: медикаментозное и физиотерапевтическое лечение, которое позволяет получить положительные результаты практически у всех больных. Проводим лечение больных с постмастэктомическим синдромом с помощью курсового применения лазеро- и фототерапии в виде воздействия на мягкие ткани отечной конечности некогерентным монохроматическим световым излучением светодиодной матричной установки.
Этот прибор был разработан в тесном сотрудничестве нашей кафедры с кафедрой биомедицинских технических систем МГТУ им. Н.Э. Баумана. Первоначально, десять лет назад, мы начали с разработки матричного лазера, первый экземпляр которого собрали своими руками. Сегодня, после проведения надлежащих испытаний и регистрации в Министерстве здравоохранения и социального развития РФ, прибор выпускается заводским методом в четырех модификациях (красного и инфракрасного света) с мягким и жестким каркасом. Красный свет необходим при воздействии на капиллярную сеть и на кровь, а инфракрасное излучение используется при обработке мягких тканей, обеспечивая резорбцию рубцовой ткани.
Как известно, традиционное лечение больных с постмастэктомическим отеком часто бывает неэффективным. С помощью нашего прибора мы получаем терапевтический эффект даже у тех больных, которым не приходилось надеяться на сколько-нибудь успешную реабилитацию, и это не требует серьезных финансовых и временных затрат. Воздействие этим прибором позволяет улучшить кровообращение и восстановить деятельность мозга, что мы доказали в многочисленных исследованиях, где подтвердили следующий факт: некогерентное монохроматическое лазерное излучение не столько направлено на лечение человека, сколько заставляет организм находить компромиссное решение по компенсации всего комплекса нарушений. По большому счету — это оптимальная коррекция состояния организма больного. Для большей эффективности восстановительной терапии мы начинаем проводить воздействие лазером уже в раннем послеоперационном периоде.
Л.В.: Мы также производим лечение с применением различных компрессионных изделий, когда применяется дозированная компрессия на руку. Также еще в процессе операции больной ставится специальная гофрированная компрессионная банка, которая всасывает лимфу, разработаны различные давящие повязки. Лечение таких больных — это целый комплекс мероприятий, позволяющих облегчить их существование.
Важно понимать, что успешное лечение этих пациентов возможно лишь в тесном сотрудничестве с врачами других специальностей (неврологами, физиотерапевтами).
— Сегодня имеется достаточно много данных о качестве жизни больных с теми или иными заболеваниями. Проводилось ли изучение данного вопроса у пациенток с постмастэктомическим синдромом?
М.С.: Совместно с кафедрой неврологии МГМСУ проводили оценку качества жизни этих больных с помощью специальных тестов, разработанных сотрудниками нашей клиники. Были получены данные: больные, которым поставлен диагноз “рак молочной железы”, в течение всей жизни (до радикального лечения и после него) ощущают сильнейшую депрессию, угнетение деятельности центральной нервной системы, у них развивается настоящий депрессивный психоз. К концу первого года жизни после операции примерно у 80% больных развивается депрессивный психоз разной степени выраженности. К примеру, мы исследовали электроэнцефалограммы таких больных. Во время проведения этой процедуры давали определенную нагрузку на пораженную конечность и оценивали результаты, при этом наибольший всплеск отмечался именно в тех зонах, которые ответственны за эмоциональное состояние человека. Даже при элементарном заборе крови отмечалась разница в показателях агрегации тромбоцитов из проб на здоровой и пораженной руке. В конечности со стороны мастэктомии вязкость крови увеличена в несколько раз. Как я уже отмечал, с помощью монохромного лазерного излучения удается добиться коррекции этих нарушений. Было замечено, что после того курса реабилитационной терапии больные отмечают резкое улучшение самочувствия: повышение эмоционального фона и общего жизненного тонуса, возникает стремление к активной деятельности. Однако по истечении определенного времени, примерно через 3—4 мес, указанные проблемы вновь начинают их беспокоить. Это требует повторного курса восстановительной терапии.
— А что можете сказать по поводу проведения реконструктивных операций на лимфатических и кровеносных сосудах таким больным?
М.С.: Относительно реконструктивных пластических операций хотелось бы сказать следующее: на 5—10-й день после ее проведения больные обычно отмечают резкое улучшение состояния, а вот спустя два года или чуть более у таких пациентов наступают уже необратимые рубцовые изменения в мягких тканях и ухудшение общего самочувствия, коррекция которого, как правило, малоэффективна, поскольку реконструктивная операция — это прежде всего новая травма, новые рубцы, которые на фоне проведенной лучевой терапии и старых рубцов выводят патологический процесс в целом на новый, более тяжелый этап развития.
— Скажите, отличаются ли подходы к лечению в нашей стране и за рубежом?
Л.В.: В большинстве зарубежных стран в отличие от России на этапе реабилитации в основном используются компрессионные и медикаментозные методы, а воздействие физическими факторами, такими как лазерное излучение, фототерапия, отсутствует, что делает нас лидерами в этой области лечения больных с данной патологией.
Постмастэктомический синдром
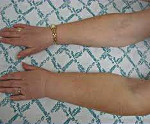
Постмастэктомический синдром — комплекс специфических симптомов, возникающий у пациенток, перенесших радикальную мастэктомию. Проявляется отеком, изменениями кожи, неврологическими и двигательными расстройствами в руке на стороне удаленной груди, депрессией. При постановке диагноза используют результаты физикальных исследований, лимфосцинтиграфии, дуплекс-сонографии, электронейромиографии. Для лечения применяют физиотерапевтические и физические методы (пневматическую компрессию, лимфодренаж и др.), дополненные препаратами с вазоактивным и лимфодренирующим эффектом. В исключительных случаях иссекают измененные ткани, выполняют микрососудистые операции.
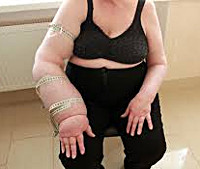
- Причины постмастэктомического синдрома
- Патогенез
- Классификация
- Симптомы постмастэктомического синдрома
- Осложнения
- Диагностика
- Лечение постмастэктомического синдрома
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Постмастэктомический отек верхней конечности с комплексом характерных трофических, нейромоторных и психических симптомов — одно из наиболее частых осложнений радикальных операций по поводу злокачественных неоплазий молочной железы. По наблюдениям специалистов, синдром возникает у 16,8-64,6% перенесших мастэктомию. Длительность периода между хирургическим вмешательством и временем появления клинических симптомов в среднем составляет от 10 до 24 месяцев, однако возможна и более поздняя манифестации симптоматики (через 10 и более лет). Статистически чаще расстройство поражает пациенток, у которых удалена правая грудь. Актуальность своевременного выявления патологии обусловлена существенным ухудшением качества жизни и инвалидизацией женщин на поздних стадиях заболевания.

Причины постмастэктомического синдрома
Специфический симптомокомплекс, характерный для больных, перенесших хирургическое вмешательство по поводу рака молочной железы, формируется в раннем послеоперационном и восстановительном периоде на фоне травматических повреждений, реологических и сосудистых нарушений. Выраженность расстройств связана с особенностями репарационных процессов, техникой выполнения и объемом операции, течением послеоперационного периода. Непосредственными причинами постмастэктомического синдрома являются:
- Нарушение сосудистой микроциркуляции. При радикальных методах мастэктомии удаляют подмышечный, подключичный, подлопаточный коллекторы. Это приводит к ухудшению оттока лимфы на стороне поражения. Ситуация усугубляется длительным спазмом сосудов с последующим тромбированием и воспалением (лимфангиитом, тромбофлебитом).
- Рассечение нервных волокон. Во время операции повреждаются многочисленные мелкие нервы, которые обеспечивают иннервацию сосудов и тканей в области шеи, плечевого пояса, руки. Это ухудшает восстановительные постмастэктомические процессы, вызывает болевые ощущения и специфические нарушения чувствительности, получившие название скаленус-синдрома.
- Удаление грудных мышц. Некоторые виды операций при раке молочной железы предполагают резекцию малой и большой грудных мышц на стороне опухоли. Результатом таких вмешательств становится существенное ограничение движений в плече с формированием контрактуры. Патология наблюдается практически у 40% прооперированных.
- Рубцовые изменения тканей. После удаления молочной железы, особенно в случаях, когда оно сопровождается пред- и послеоперационной радиотерапией, в области грудной клетки и подмышечной впадине происходит рубцевание. Выраженность фиброзной деформации увеличивается, если послеоперационный период протекал с гнойно-некротическими осложнениями.
По данным специалистов в сфере маммологии, частота и тяжесть постмастэктомических расстройств зависят от размеров опухоли, степени вовлечения в процесс аксиллярных лимфоузлов, наличия метастазов. Вероятность развития синдрома повышается при распространенности опухолевого процесса, неправильном определении объема операции, нарушении ее техники, неадекватной послеоперационной и лучевой химиотерапии.
Патогенез
Механизм формирования постмастэктомического синдрома основан на изменениях реологических параметров, сосудистой и перисосудистой реакции в пораженной области. Патогенез включает несколько звеньев. В сосудах на пораженной стороне повышается агрегация тромбоцитов, что приводит к спазму и микротромбозам. На фоне нарушенной микроциркуляции развивается перикапиллярный отек. Поскольку амплитуда движений руки на стороне операции ограничена, микронасосная функция скелетных мышц ухудшается. В результате кристаллоиды, белки и вода из межтканевой жидкости медленнее всасываются в микроартериолы, начинают скапливаться в виде отека. Дополнительными факторами патогенеза становятся нейротрофические нарушения и послелучевой фиброз тканей, окружающих магистральные сосуды, что вызывает сужение последних.
Классификация
Единая систематизация форм постмастэктомической патологии пока отсутствует. Большинство предложенных классификаций основано на выраженности отека тканей. При этом авторы учитывают время развития расстройств (ранние, возникшие до 3 месяцев после мастэктомии, и поздние, с отсроченным началом проявлений), плотность тканей (мягкие, твердые, деформированные), изменение объемов. При разнице между обхватом плеча, измеренным над локтем пораженной и здоровой руки, отек до 2 см расценивается как легкий, от 2 до 6 см — средний, свыше 6 см — тяжелый. Российские маммологи и онкологи часто пользуются классификацией постмастэктомического синдрома, основанной на клинических признаках:
- I степень. Отечность локализована в дистальных сегментах пораженной руки (пальцы, кисть), возникает эпизодически. Объем отекшей верхней конечности превышает объем здоровой менее чем на 25%. Снижена температура кожи кисти.
- II степень. В отек вовлечены мягкие ткани предплечья. Кожные покровы трудно захватить в складку. Увеличение объема пораженной руки составляет от 25% до 50%. Отмечается локальное понижение температуры в области кисти и предплечья.
- III степень. Отечность поднимается на плечо и держится постоянно. Ткани плотные, кожа и подкожная клетчатка фиброзно изменены, склерозированы. Кожа не берется в складку. Объем увеличен на 50-70%. Температура кожи снижена в области предплечья и кисти.
- IV степень. Рука деформирована, движения ограничены. Выявляются трофические поражения кожных покровов. Объем пораженной конечности увеличен на 70% и больше. Регистрируется снижение температуры не только на кисти и предплечье, но и на плече.
Существует также комплексная классификация, предложенная отечественными учеными. Она максимально учитывает выраженность отека, время его появления, постоянство, этапность развития, наличие эстетических нарушений, сопутствующей патологии и осложнений, их влияние на привычный образ жизни прооперированной женщины. На основании этих критериев различают следующие стадии постмастэктомического симптомокомплекса:
- Доклиническая стадия. Внешние проявления отечности отсутствуют на протяжении всего дня. Увеличение объема поврежденной верхней конечности не превышает 150,0 мл. Длина окружности плеча не изменена. Субъективных жалоб нет. Цвет кожи нормальный. Кожные покровы хорошо берутся в складку.
- Начальная стадия. Непостоянный отек отдельных сегментов или всей верхней конечности возникает преимущественно к вечеру. Увеличение объема 150-300 мл, окружности плеча — 1-2 см. Пациентка жалуется на тяжесть, периодические боли. Кожа берется в более грубые складки, теряет здоровый цвет.
- Стадия умеренных нарушений. Отечность держится постоянно, не проходит после ночного сна. Пораженная рука увеличивается на 300-500 мл в объеме и на 4-6 см в обхвате плеча. Кожные покровы сложно взять в складку. Они выглядят бледными, появляется синюшный оттенок.
- Стадия выраженных нарушений. Постоянная отечность переходит в плотную фибредему. Объем конечности возрастает на 500-700 мл. Увеличение обхвата плеча — не больше 6 см. Наблюдается деформация тканей с частичной утратой функции конечности. Пациентка испытывает парестезии, боли.
- Отягощенный постмастэктомический отек. Объем верхней конечности увеличивается на 700 мл и больше, окружность плеча — более чем на 6 см. Рука фактически не функционирует, большую часть времени вынужденно подвешена на повязку. Выражены трофические расстройства.
Симптомы постмастэктомического синдрома
Ключевым проявлением симптомокомплекса является постепенно нарастающая отечность мягких тканей, из-за чего эта патология раньше называлась постмастэктомическим отеком (ПМО). Заболевание крайне редко развивается сразу после операции. Обычно первые признаки отечного синдрома клинически определяются спустя несколько месяцев и даже лет после вмешательства. На начальных этапах болезни к вечеру отекают дистальные сегменты верхней конечности (пальцы, кисть), пациентке трудно надеть или снять обручальное кольцо и привычные ювелирные украшения. За ночь отечность полностью проходит. В кисти может возникать ощущение тяжести. По мере развития посмастэктомического синдрома отек поднимается выше — на предплечье, плечо, надплечье, в далеко зашедших случаях он охватывает надключичную область, шею, верхнюю часть грудной клетки.
Сначала кожа над отечными участками сохраняет обычную окраску. Со временем она становится бледной, цианотичной, сухой, шелушащейся. Локальная температура снижается на 0,5-1° С. Постепенно мягкие ткани уплотняются, кожная складка формируется плохо, возможны трофические поражения. Более чем у половины пациенток с постмастэктомическими нарушениями нарушена чувствительность — возникает чувство онемения, ползания мурашек. Интенсивность болевого синдрома варьируется, женщина может ощущать как незначительную тупую, так и продолжительную тупую или кратковременную жгучую боль с иррадиацией в плечо, шею, грудную клетку. Двигательные расстройства представлены ограничением подвижности в плечевом суставе различной степени выраженности. Почти у четверти пациенток диагностируют тяжелую депрессию.
Осложнения
Длительно существующий постмастэктомический синдром может спровоцировать тендовагинит и другие поражения надостной мышцы, хронический бурсит, почти в 40% случаев ограничивающий движения рукой и приводящий к формированию контрактуры. У 1,5-11% пациенток возникают брахиоплекситы и полинейропатические расстройства. Больше чем у 99% прооперированных с такой патологией диагностируется скаленус-синдром. При отеке III-IV степени повышается вероятность рожистого воспаления. В ряде случаев хронический лимфостаз осложняется синдромом Стюарта-Тривса (возникновением лимфангиосаркомы). Поскольку посмастэктомические нарушения негативно сказываются на профессиональной пригодности женщины, их развитие сопровождается снижением самооценки, нарастанием невротической симптоматики и депрессивного синдрома.
Диагностика
При диагностике постмастэктомических нарушений в первую очередь учитывают данные физикальных исследований — оценивают объем здоровой и пораженной конечностей, их обхват над локтевым суставом, определяют кожную температуру для выявления степени ее снижения, проверяют чувствительность кожи и амплитуду движений в плече. Инструментальные методы исследования позволяют верифицировать уровень повреждения сосудистого русла, оценить функциональную состоятельность тканей. Чаще всего назначают следующие исследования:
- Лимфосцинтиграфия верхних конечностей. Радиоизотопный метод, пришедший на смену традиционной лимфографии, визуализирует особенности строения лимфатической системы, выявляет участки застоя лимфы и объективизирует снижение скорости лимфотока.
- Дуплексное сканирование. Сочетанное проведение ультразвукового и допплерографического исследования направлено на определение скорости кровотока, анатомических особенностей и проходимости артериальных и венозных сосудов.
- Электронейромиография. Методика позволяет объективно оценить функциональное состояние периферических нервов, иннервирующих кожу, мышцы и сосуды верхних конечностей, диагностировать выраженность неврологических расстройств.
В ходе комплексного обследования выполняют лабораторные анализы для оценки системы гемостаза, в сложных клинических случаях проводят МРТ, КТ. Дифференциальная диагностика заболевания, как правило, не представляет особых сложностей с учетом возникновения нарушений после мастэктомии. Несмотря на очевидность причин развития постмастэктомического синдрома, необходимо сохранять настороженность в отношении других причин лимфостаза — доброкачественных и злокачественных опухолей лимфатической системы, воспалительных сосудистых заболеваний. При необходимости к обследованию пациентки привлекают хирурга, онколога, лимфолога, флеболога, невропатолога, дерматолога, инфекциониста.
Лечение постмастэктомического синдрома
Врачебная тактика при развитии отека, неврологических и двигательных расстройств после мастэктомии направлена на восстановление нарушенных функций — облегчение лимфодренажа, разработку плечевого сустава, нейростимуляцию. Ведущей является комплексная консервативная терапия, которая лишь в крайних случаях дополняется хирургическими методиками. Пациенткам с постмастэктомической болезнью назначают:
- Физические и физиотерапевтические воздействия. Наиболее эффективны аппаратная пневматическая компрессия руки от пальцев и кисти до надплечья, ручной и механический лимфодренаж. Эти методики дополняют специальными физическими упражнениями, ношением бандажей, многослойных неэластичных и эластических повязок. Предварительное применение ультразвука позволяет «размягчить» ткани, уменьшить остеомиофасциальные боли, улучшить чувствительность и подвижность в суставах. Некоторые специалисты получили хорошие терапевтические результаты при использовании световой и низкоуровневой лазеротерапии, электромиостимуляции.
- Медикаментозное лечение. Из фармакологических средств при послемастэктомическом синдроме часто назначают бензопироны — препараты с вазоактивным, антиэдематозным и противовоспалительным эффектом. Для усиления их действия применяют ангиопротекторы, капилляростабилизаторы, антиагреганты, витамины с антиоксидантным действием. Хороший эффект в купировании болевого синдрома и коррекции нейродвигательной патологии достигается при введении психоаналептиков и протеолитических ферментов. При выраженной боли и эмоциональных расстройствах допустимо использование седативных и нестероидных противовоспалительных средств.
- Хирургические методы. Оперативный подход к устранению постмастэктомического лимфостаза практикуется редко. В ходе хирургической коррекции иссекается рубцовая ткань с замещением дефекта собственной кожей или кожно-мышечным лоскутом пациентки. Микрососудистые техники позволяют сформировать лимфовенозные анастомозы, освободить от сращений подключичную и подмышечную вены. Возможности хирургического лечения у больных с нарушениями после мастэктомии ограничены многостадийностью, травматичностью, сложностью технического исполнения, достижения стойких функциональных и косметических результатов.
Прогноз и профилактика
Несмотря на высокую терапевтическую резистентность расстройства, комплексный подход и своевременное начало лечения на ранних стадиях постмастэктомического синдрома позволяют уменьшить выраженность отека и улучшить функциональные возможности пораженной руки. С профилактической целью необходимо обоснованно определять вид и объем вмешательства при злокачественном новообразовании груди, тщательно соблюдать технику выполнения операции. В конце первой недели послеоперационного периода показаны дозированные упражнения для разработки плечевого сустава, с 3 недели — самомассаж мышц и кожи. В последующем женщине рекомендуются умеренные физические нагрузки, исключение сдавливаний руки, ее защита от возможной травматизации на производстве или в быту.