Болезнь Брутона (агаммаглобулинемия): что это такое?

Х-сцепленная агаммаглобулинемия (болезнь Брутона), первичное нарушение гуморального иммунитета, связанное с дефектом гена, кодирующего тирозинкиназу Брутона. Данный фермент берет участие в созревании и дифференцировке В-лимфоцитов (клетки, продуцирующие антитела). При его дефекте в крови отсутствуют зрелые В-лимфоциты и практически полностью отсутствуют плазмоцитарные клетки (разновидность В-лимфоцитов, продуцирующих антитела) и иммуноглобулины (антитела).
Заболевание открыл Огден Брутон, педиатр из США в 1952 году как одно из первых иммунодефицинтых заболеваний. Пациентом был ребенок 8 лет с иммуносупресией, который за 4 года перенес 14 случаев пневмонии, менингит, постоянно страдал синуситами, отитом, и переболел сепсисом. В плазме его крови практически отсутствовали антитела.
В 1993 году учёные открыли молекулярно-генетический механизм патологии, суть которого заключалась в мутации гена, кодирующего фермент тирозинкиназу. Данный энзим входит в состав многих клеток костномозгового происхождения (моноциты, эритробласты, базофилы, нейтрофилы), но его дефект вызывает изменения только в В-лимфоцитах. Поэтому он и получил название «тирозинкиназа Брутона».
Наследование
Агаммаглобулинемии Брутона характерен Х-сцепленный рецессивный тип наследования: болеют только мальчики. Девочки не склонны к заболеванию, даже если они гетерозиготны (здоровый ген компенсирует мутированный Х-рецессивный ген). Частота встречаемости патологии 10:25 000.
Клиническая картина
Болезнь манифестирует в раннем грудном возрасте, чаще всего в 3–4 месяца, и связана со снижением концентрации материнских антител в крови младенца. Характерными проявлениями болезни есть постоянно рецидивирующие инфекции, спровоцированные гемофильной палочкой, стрептококками или пневмококками. При вакцинации против полиомиелита живой вакциной возможно развитие клинической формы полиомиелита. Вакцинация против гепатита В может спровоцировать развитие его фульминантной (сверхострой) формы. Перенесённые острые кишечные инфекции могут спровоцировать развитие синдрома мальабсорбции — нарушение всасывания в тонком кишечнике, которое проявляется хроническими диареями. Первичные очаги поражения возникают в лёгких, придаточных пазухах носа.
- желудочно-кишечный тракт;
- лёгкие и верхние дыхательные пути;
- суставы;
- кожа.
Часто встречаются эпизоды следующих заболеваний:
- хроническая диарея (вследствие развития мальабсорбции);
- конъюнктивит;
- воспаления среднего уха;
- дерматиты, пиодермии;
- бронхиты, фаригниты;
- хронические синуситы (воспаление придаточных пазух носа);
Характерным есть поражения центральной нервной системы в виде энцефалитов, менингитов, склонность к аутоиммунным заболеваниям, злокачественным новообразованиям. Ещё одним часто встречающимся заболеванием при Х-сцепленой агаммаглобулинемии есть ревматические проявления с характерным суставным синдромом. Артралгии поражают большие суставы, имеют мигрирующий характер и даже при длительном течении не провоцируют развитие рентгенологических изменений в суставах.
Диагноз
Ранняя диагностика имеет важное значение для предотвращения развития вторичных инфекций и снижает процент летальности от болезни. Диагноз подтверждается аномально низким уровнем зрелых В-клеток лимфоцитарного ряда. В протеинограмме отсутствуют гаммаглобулины. В костном мозге критически снижены или отсутствуют плазмоциты. В общем анализе крови лейкопения или лейкоцитоз. Сильно снижены уровни IgA, IgМ и IgG в плазме крови. При молекулярно-генетическом исследовании определяют дефект длинного плеча Х хромосомы. Это обследование рекомендуют провести всем женщинам семьи для определения носительства патологии.

Морфологические изменения в первую очередь касаются селезёнки и лимфатических узлов (в лимфоузлах сужен кортикальный шар и недоразвиты фолликулы). Лимфоидная ткань всего организма либо недоразвита или отсутствует, также отсутствуют миндалины.
В редких случаях диагноз агаммаглобулинемии Брутона устанавливают на втором десятке жизни человека. В таких случаях речь идет не об отсутствии тиррозинкиназы, а мутации в её структуре. Иммуносупресия при этом не полная.
Дифференциальную диагностику важно провести с агаммаглобулинемией швейцарского типа. При болезни Брутона в крови будут отсутствовать только В-лимфоциты, а при агаммаглобулинемии швейцарского типа отсутствуют и Т- и В-лимфоциты.
Лечение
Патогенетическим лечением агаммаглобулинемии есть заместительная терапия. Пациентам внутривенно или внутримышечно вводят иммуноглобулины — препараты, содержащие антитела, которые клетки пациента не способны синтезировать. Данное лечение проводят пожизненно. Симптоматическая терапия состоит из введения антибиотиков и при необходимости дезинтоксикационной терапии.
Прогноз
Прогноз нелеченной агаммаглобулинемии неблагоприятный, болезнь заканчивается летальным исходом от тяжелых инфекций. Если же проводится необходимая терапия, то данные пациенты остаются склонны к развитию аутоиммунных заболеваний, рецидивов инфекций, формирования хронических очагов инфекций, высокого риска развития онкологической патологии.
Профилактика
Причиной болезни Брутона является генетический дефект фермента, поэтому профилактировать появлении болезни невозможно. Основные меры профилактики направлены на избежание частых рецидивов вторичных инфекций и осложнений болезни. К ним относят:
Агаммаглобулинемия: что это такое, и как лечить

Что такое агаммаглобулинемия?

Отсутствие гаммаглобулинов имеет первичный характер
Агаммаглобулинемией называется наследственное заболевание, которое характеризуется развитием первичного иммунодефицита по причине полного отсутствия в организме больного иммунных белков — антител.
Первым пациентом с диагностированным отсутствием в сыворотке крови антител, стал мальчик восьми лет, который за последние четыре года своей жизни болел инфекционными заболеваниями в сумме около двадцати раз. Тяжёлые пиодермии, пневмонии, отиты, менингиты и септические состояния возникали по причине неспособности организма противостоять инфекционным агентам, купировать вирусный и бактериальный процесс.
Белки сыворотки крови человека бывают нескольких типов: альбумины и большая группа глобулинов, среди которых можно выделить подгруппы альфа-1, альфа-2, бета и гамма. Первые три подгруппы включают, в основном, ферменты, белки свёртывающей и фибринолитической системы крови, липопротеины, компоненты комплемента, в отличие от них подгруппа гамма-глобулинов менее разнообразная, она включает только лизоцим и иммуноглобулины классов A, M, G, E, D, выполняющие гуморальную защиту организма.
Причины агаммаглобулинемии

К развитию заболевания приводит геномная мутация
Только в конце 20 века была установлена главная причина заболевания — мутация гена, локализованного на Х-хромосоме. Этот ген содержит код фермента тирозинкиназы, необходимого для формирования предшественников В-лимфоцитов в красном костном мозге. Частота мутации в популяции составляет 1 случай на 200000 детей.
Так как тип наследования Х-сцепленный и рецессивный, заболевание проявляется только у мальчиков, имеющих, в отличие от девочек, всего одну Х-хромосому, поэтому мутация гена на этой хромосоме всегда имеет клиническое значение. Больные наследуют эту хромосому у матерей, являющихся гетерозиготными носительницами повреждённого гена. То есть одна из их Х-хромосом имеет нормальный генетический код, а вторая Х-хромосома — повреждённый. При этом клинически матери здоровы и не подозревают о носительстве дефектного гена.
На молекулярном уровне ген может быть повреждён в разной степени. Возможна замена нескольких нуклеотидов в цепочке ДНК, что приводит к прекращению синтеза необходимых аминокислот в составе тирозинкиназы и создаёт мало функциональный фермент. В этом случае возможна наработка минимального количества иммуноглобулинов в организме, но свои функции они смогут выполнять с трудом. Более массивные мутации (например, делеции) могут привести к полному прекращению синтеза тирозинкиназы и, соответственно, иммунных белков организма.
Патогенез заболевания

Геномная мутация ведет к синтезу дефектной тиронкиназы
Вследствие мутации гена и образования дефектной тирозинкиназы последняя не стимулирует рост и созревание предшественников В-лимфоцитов в костном мозге, происходит остановка их развития на уровне пре-В-лимфоцитов, юных форм. Эти клетки не попадают в сосудистое русло, не преобразуются в плазмоциты, ответственные за синтез иммуноглобулинов в ответ на вторжение в организм возбудителей инфекций, и клетки памяти, необходимые для более быстрой реакции организма на уже известный антиген. В итоге нарушается гуморальный иммунитет, в большей степени направленный на борьбу с вирусами. Бактериальные инфекции обычно играют роль осложнений, так как клеточный иммунитет (Т-лимфоциты, макрофаги) при данной патологии не страдает.
Классификация
Можно выделить три формы этой патологии:
- Агаммаглобулинемия, сцепленная с Х-хромосомой, она встречается практически у 90% больных детей, заболеванию подвержены только мальчики.
- Агаммаглобулинемия, сцепленная с некоторыми аутосомными (неполовыми) генами, встречается не более, чем в 2-3% случаев, причём как у мальчиков, так и у девочек.
- Агаммаглобулинемия, сцепленная с Х-хромосомой и гипопродукцией соматотропина, встречается крайне редко, только у мальчиков.
Симптомы и признаки агаммаглобулинемии

Начало проявлений заболевания у детей — 5-7 лет
Для этой патологии характерны повторные, длительно текущие, плохо поддающиеся лечению, тяжёлые инфекционно-воспалительные процессы в организме.
В первые 6-9 месяцев жизни в кровотоке новорождённого циркулируют иммуноглобулины, полученные от матери через сосуды плаценты и с грудным молоком (IgA, главным образом), поэтому явной клиники агаммаглобулинемии нет, наиболее яркие её проявления отмечают с двух до пяти-семи лет. В это время родители обращают внимание на частые инфекционные заболевания у ребёнка, вскоре принимающие характер хронического процесса, и начинают поиск причины.
Общие симптомы: лихорадка, озноб, потливость, плохой аппетит, уменьшение массы тела, раздражительность, либо угнетение, сонливость.
Поражения кожи и подкожной клетчатки: пиодермия, экзема, фурункулы, карбункулы, абсцессы, флегмоны.

В патологический процесс могут вовлекаться любые органы
Поражения ротовой полости, глаз, органа слуха, пазух черепа: ангины, язвы слизистой рта, фарингиты, гнойные и вирусные конъюнктивиты, отиты, гаймориты, фронтиты и прочие синуситы вплоть до поражения всех пазух — пансинусита.
Поражения лёгких, сердца, кишечника: вирусные и бактериальные пневмонии, плевриты, миокардиты, бактериальные эндокардиты, энтероколиты, проктиты, парапроктиты.
Поражения почек и мочевыделительной системы: пиелонефриты, циститы, уретриты, вульвовагиниты у девочек.
Поражения костей: гнойный остеомиелит, артриты.
Поражения нервной системы: менингиты, энцефалиты, полиомиелит.
Критические состояния: кома, сепсис, дыхательная, сердечная, почечная недостаточность.
Диагностика заболевания

Пациенты подлежать всестороннему обследованию
- Анализы крови, мочи, ликвора, свидетельствующие о воспалении и инфекционном процессе. Например, нейтрофильный лейкоцитоз, лимфопения, увеличение СОЭ, высокий нейтрофильный цитоз спинномозговой жидкости, лейкоциты и белок в моче.
- Протеинограмма — процентное соотношение разных фракций белков сыворотки крови. Вся фракция гамма-глобулинов отсутствует, либо значительно снижена.
- Миелограмма — анализ оценки морфологической картины костного мозга. Количество зрелых В-лимфоцитов снижено, но имеются пре-В-лимфоциты в большом количестве.
- Биопсия лимфоузлов и селезёнки: кортикальный слой, образуемый В-лимфоцитами, значительно сужен, плохо развиты первичные фолликулы. Так же отмечают уменьшение лимфоузлов и глоточных миндалин в размерах.
- Генетическое исследование: поиск мутации гена на Х-хромосоме. Возможно обследование родителей, братьев и сестёр ребёнка на носительство изменённых генов.
Лечение

Пациентам может понадобиться госпитализация
Лечением пациента занимается врач иммунолог и инфекционист.
Необходима пожизненная коррекция недостатка иммуноглобулинов путём введения в вену гамма-глобулинов или донорской плазмы.
Если заболевание диагностировано впервые, лечение проводится в режиме насыщения: гамма-глобулин вводится до общей массы его 3 г/л, но удобнее дозировать препарат по 200-400 мг на кг массы тела. Препарат вводят с интервалом 2-4 недели. Контроль уровня гамма-глобулинов, как правило, ведут по уровню IgG в сыворотке. После насыщения нужна пожизненная поддерживающая терапия профилактическими дозами препарата.
В случае инфекционного заболевания любой локализации необходима обязательная госпитализация пациента, повышение доз вводимых иммуноглобулинов, адекватная антибактериальная и противовирусная терапия. Наиболее современными антибиотиками считаются макролиды, фторхинолоны, новые поколения цефалоспоринов, иногда прибегают и к аминогликозидам, всё реже — к антибиотикам пенициллинового ряда.
В зависимости от локализации процесса используются препараты для поддержки повреждённого органа, антисептики, инфузионная терапия.
Прогноз

Своевременная диагностика и лечение дают хорошие прогнозы
При своевременной диагностике и корректировке состояния острая клиника купируется, однако могут остаться хронические изменения в органах, что во взрослом возрасте может привести к снижению трудоспособности.
В неблагоприятных социальных условиях при отсутствии доступа к современным методам исследования и лечения многие дети могут погибнуть от осложнений в первые два-три года жизни.
Агаммаглобулинемия ( Болезнь Брутона , Наследственная гипогаммаглобулинемия )

Агаммаглобулинемия – это наследственно обусловленное заболевание, при котором развивается тяжелый первичный иммунодефицит (дефект иммунной защиты организма) с выраженным снижением уровня гамма-глобулинов в крови. Проявляется болезнь обычно в первые месяцы и годы жизни ребенка, когда начинают развиваться повторные бактериальные инфекции: отит, синусит, пневмонии, пиодермии, менингит, сепсис. При обследовании в периферической крови и костном мозге практически отсутствуют сывороточные иммуноглобулины и B-клетки. Лечение агаммаглобулинемии заключается в пожизненной заместительной терапии.
МКБ-10
- Причины
- Классификация
- Симптомы агаммаглобулинемии
- Осложнения
- Диагностика
- Лечение агаммаглобулинемии
- Прогноз
- Цены на лечение
Общие сведения
Агаммаглобулинемия (наследственная гипогаммаглобулинемия, болезнь Брутона) – врожденный дефект гуморального иммунитета, обусловленный мутациями в геноме клеток, что приводит к недостаточности синтеза B-лимфоцитов. В результате нарушается образование иммуноглобулинов всех классов, и их содержание в крови резко снижается вплоть до полного отсутствия, развивается первичный иммунодефицит. Низкая реактивность иммунной системы приводит к развитию тяжелых повторных гнойно-воспалительных заболеваний ЛОР-органов, бронхов и легких, желудочно-кишечного тракта и мозговых оболочек. Болезнь Брутона встречается исключительно у мальчиков и наблюдается примерно у 1-5 человек из миллиона новорожденных, независимо от расы и этнической группы.

Причины
X-сцепленная форма наследственной агаммаглобулинемии возникает вследствие повреждения одного из генов X-хромосомы (расположен на Xq21.3-22.2). Этот ген ответственен за синтез фермента тирозинкиназы, участвующего в процессе образования и дифференцировки B-клеток. В результате мутаций этого гена и блокировки синтеза брутоновской тирозинкиназы нарушается формирование гуморального иммунитета. При агаммаглобулинемии молодые формы (пре-B-клетки) присутствуют в костном мозге, а их дальнейшая дифференцировка и поступление в кровеносное русло нарушена.
Соответственно, выработка всех классов иммуноглобулинов практически не производится, и организм ребенка становится беззащитным при проникновении болезнетворных бактерий (чаще всего это стрептококки, стафилококки и синегнойная палочка). Сходный механизм нарушений отмечается и в случае с другой формой наследственной агаммоглобулинемии — сцепленной с X-хромосомой и недостаточностью гормона роста. Аутосомно-рецессивная форма развивается в результате мутации нескольких генов (µ-тяжелых цепей, гена λ5/14.1, гена адапторного белка и гена сигнальной молекулы IgА).
Классификация
Выделяют три формы наследственной агаммаглобулинемии:
- сцепленная с X-хромосомой (85% всех случаев врожденных гипогаммаглобулинемий, болеют только мальчики)
- аутосомно-рецессивная спорадическая швейцарского типа (встречается у мальчиков и девочек)
- сцепленная с X-хромосомой и недостаточностью гормона роста агаммаглобулинемия (встречается крайне редко и только у мальчиков)
Симптомы агаммаглобулинемии
Сниженная реактивность гуморального иммунитета при агаммаглобулинемиях приводит к развитию повторных гнойно-воспалительных заболеваний уже на первом году жизни ребенка (как правило, после прекращения грудного вскармливания – в 6-8 месяцев). При этом защитные антитела от матери в организм ребенка уже не поступают, а свои иммуноглобулины – не вырабатываются. К 3-4 летнему возрасту воспалительные процессы переходят в хроническую форму со склонностью к генерализации. Гнойная инфекция при агаммаглобулинемии может поражать различные органы и системы.
Со стороны ЛОР-органов нередки гнойные гаймориты, этмоидиты, отиты, причем гнойный отит чаще развивается на первом году жизни ребенка, а синуситы – в 3-5 лет. Из заболеваний бронхолегочной системы наблюдаются повторные бронхиты, пневмонии, абсцессы легкого. Часто встречается поражение желудочно-кишечного тракта с упорной диареей (поносами), вызванной хроническим инфекционным энтероколитом (основные возбудители – кампилобактерии, лямблии, ротавирус). На кожных покровах обнаруживается импетиго, микробная экзема, рецидивирующий фурункулез, абсцессы и флегмоны.
Нередким бывает поражение глаз (гнойные конъюнктивиты), полости рта (язвенные стоматиты, гингивиты), костно-мышечной системы (остеомиелиты, гнойные артриты). В целом клиническая картина агаммаглобулинемии характеризуется сочетанием общих симптомов, наблюдаемых при гнойной инфекции (высокая температура тела, озноб, боли в мышцах и головная боль, общая слабость, нарушение сна и аппетита и т. д.) и признаков поражения конкретного органа (кашель, одышка, затруднение носового дыхания, гнойное отделяемое, диарея и т. п.).
Осложнения
Любое инфекционное и соматическое заболевание у больного иммунодефицитом протекает тяжело, длительно и сопровождается осложнениями. Тяжелое течение агаммоглобулинемии может осложняться развитием менингита, вирусного энцефаломиелита, поствакцинального паралитического полиомиелита, сепсиса. На фоне заболевания повышена вероятность развития аутоиммунных и онкологических заболеваний. Гибель пациентов часто наступает от инфекционно-токсического шока.
Диагностика
При клиническом осмотре пациента врачом аллергологом-иммунологом выявляются признаки гнойно-воспалительного поражения того или иного органа (ткани) и симптомы, подтверждающие сниженную реактивность иммунной системы: гипоплазия миндалин, уменьшение периферических лимфатических узлов. Выражены и признаки отставания в физическом развитии ребенка.
Лабораторное исследование крови выявляет выраженное снижение уровня иммуноглобулинов в иммунограмме (IgA и IgM Автор: Мишина М.Н., врач аллерголог-иммунолог
Агаммаглобулинемия (болезнь Брутона)
Что такое агаммаглобулинемия?
Агаммаглобулинемия (болезнь Брутона) — это группа наследственных иммунодефицитов, характеризующихся низкой концентрацией антител в крови из-за отсутствия определенных лимфоцитов в крови и лимфе.
Антитела — это белки (иммуноглобулины, (IgM), (IgG) и др.), которые являются критическими и ключевыми компонентами иммунной системы. Они необходимы, если иммунная система борется с бактериями, вирусами и другими инородными веществами, которые угрожают организму. Специализированные клетки-предшественники, которые производят гамма-глобулины, не могут развиваться или функционировать должным образом, что приводит к дефициту числа зрелых лимфоцитов, называемых В-клетками.
Типы агаммаглобулинемии: X-сцепленная агаммаглобулинемия (ХСА), гораздо более редкая X-сцепленная агаммаглобулинемия с дефицитом гормона роста (зарегистрировано около 10 случаев) и аутосомно-рецессивная агаммаглобулинемия (ARAG). Все эти расстройства характеризуются ослабленной иммунной системой, которую постоянно нужно усиливать введением инъекций гамма-глобулина для борьбы с различными инфекциями.
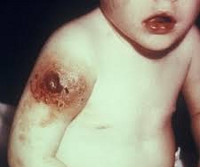
Симптомы агаммаглобулинемии
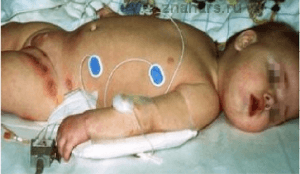
Рецидивирующие инфекции начинают развиваться в раннем детстве и сохраняются на протяжении всей взрослой жизни.
Самым частым проявлением болезни Брутона или агаммаглобулинемии является увеличение восприимчивости к инкапсулированным гнойным бактериям, к таким как гемофильные инфекции, и некоторые виды Pseudomonas. Кожные инфекции у пациентов с болезнью в основном вызываются стрептококками группы А и стафилококками, они могут проявляться в виде импетиго, целлюлита, абсцессов, или фурункулов.
Форма экземы, которая напоминает атопический дерматит может быть очевидной, наряду с увеличением числа случаев гангренозной пиодермии, витилиго, алопеции и синдрома Стивенса-Джонсона (из-за более широкого использования препаратов). Другие инфекции, которые обычно присутствуют при этой болезни, включают энтеровирусные инфекции, сепсис, менингит и бактериальный понос.
Пациенты также могут иметь аутоиммунные заболевания, тромбоцитопении, нейтропении, гемолитические анемии и ревматоидный артрит. Постоянныеэнтеровирусные инфекции очень редко приводят к смертельному энцефалиту или синдрому дерматомиозит-менингоэнцефалит. В дополнение к неврологическим изменениям, клинические проявления этого синдрома включают отеки и эритематозную сыпь на коже над разгибательными суставами.
Мужчины, могут развивать необычно тяжелый и/или периодический средний отит и пневмонии. Наиболее распространенным патогеном является S пневмония, а затем вирус гриппа B, стафилококки, менингококки и моракселла катаралис.
У детей в возрасте до 12 лет, типичные инфекции вызываются инкапсулированными бактериями. Общие инфекции в этой возрастной группе включают рецидивирующие пневмонии, синусит, и средний отит, которые вызываются S пневмония и вирусом гриппа В, которые трудно поддаются лечению в таком возрасте.
В зрелом возрасте, кожные проявления становятся более распространенными, как правило, из-за стафилококка и стрептококка группы А. Средний отит заменяется хроническим синуситом, и болезнь легких становится постоянной проблемой, как в ограничительной форме так и в обструктивной форме.
Как младенцы так и взрослые могут иметь аутоиммунные заболевания. Как правило, эти расстройства включают артрит, аутоиммунные гемолитические анемии, аутоиммунную тромбоцитопению, аутоиммунные нейтропении и воспалительные заболевания кишечника. Воспалительные заболевания кишечника могут быть очень трудно контролируемыми и они часто способствуют развитию хронической потери веса и недоеданию. Диарея является общей и вызывается лямблиями или кампилобактериозом. Пациенты склонны к энтеровирусным инфекциям, в том числе к полиовирусу.
Причины
Агаммаглобулинемия — это редкое заболевание, которым в основном болеют мужчины. Провоцируется данный недуг генетическим дефектом, в результате которого блокируется рост нормальных, сформированных иммунных клеток — B-клетки (B-лимфоциты).
В результате организм вырабатывает очень маленькое количество (а иногда и вовсе не вырабатывает) иммуноглобулинов в крови. Иммуноглобулины — играют важную роль в защите организма от разнообразных вирусов и инфекций.
Люди, страдающие от агаммаглобулинемии, часто болеют и особенно подвержены воздействию таких бактерий как: гемофильная палочка, пневмококки и стрептококки. Зачастую сопутствующие инфекции поражают:
- пищеварительный тракт;
- кожу и суставы;
- дыхательные пути.
Болезнь Брутона — заболевание, передающаяся по наследству, а это означает, что аналогичная патология может наблюдаться у других родственников больного.
Осложнения при агаммаглобулинемии
Осложнения включают хронические инфекции, энтеровирусные инфекции центральной нервной системы, увеличение частоты развития аутоиммунных заболеваний, а также инфекции кожи. Пациенты имеют повышенный риск развития лимфомы.
Диагностика
Раннее выявление и диагностика имеет важное значение для предотвращения ранней заболеваемости и смерти от системных и легочных инфекций. Диагноз подтверждается аномально низкими уровнями или вообще отсутствующими зрелыми В-лимфоцитами, а также низкой или отсутствующей экспрессией тяжелой цепи м на поверхности лимфоцитов. С другой стороны, уровень Т-лимфоцитов будет повышенным. Окончательный определитель болезни – молекулярный анализ.
Молекулярный анализ также используется для пренатальной диагностики, которая может быть выполнена с помощью отбора проб ворсинок хориона или амниоцентеза, когда мать, как известно, является носителем дефектного гена. Уровни IgG менее 100 мг/дл подтверждают диагноз.
Редко, но диагноз может быть поставлен у взрослых в их втором десятилетии жизни. Это, как полагают, происходит из-за мутации в белке, а не из-за его полного отсутствия.
Лабораторные анализы
На первом этапе необходимо провести количественное измерение IgG, IgM, иммуноглобулина Е (IgE) и иммуноглобулин А (IgA). Уровни IgG следует измерять во-первых, желательно после возраста 6 месяцев, когда уровни материнских IgG начнут снижаться. Во-вторых, уровни IgG ниже 100 мг/дл, как правило, свидетельствует о болезни Брутона. Как правило, IgM и IgA не обнаруживаются.
После того, как уровень антител будет определен как аномально низкий, подтверждение диагноза будет достигнуто с помощью анализа B-лимфоцитных и Т-лимфоцитных маркеров. Уровни CD19 + В-клеток ниже 100 мг/дл. Значения анализа Т-клеток (CD4 + и CD8 +), как правило, увеличиваются.
Дальнейший анализ может быть проведен путем обнаружения ответов IgG к Т-зависимым и Т-независимым антигенам,путем проведения иммунизации, например после введения неконъюгированной 23-валентной пневмококковой вакцины или вакцин от дифтерии, столбняка и H гриппа типа B.
Молекулярно-генетическим исследованием можно установить раннее подтверждение диагноза врожденной агаммаглобулинемии.
Другие обследования
Исследования функций легких занимают центральное место в мониторинге заболеваний легких. Они должны проводиться ежегодно у детей, которые могут выполнять тест (обычно от 5 лет).
Процедуры
Эндоскопия и колоноскопия могут быть использованы для оценки масштабов и прогрессирования воспалительного заболевания кишечника. Бронхоскопия может быть полезной в диагностике и отслеживании хронического заболевания легких и инфекций.
Лечение агаммаглобулинемии

Заместительная терапия гамма-глобулином является стандартным методом лечения агаммаглобулинемии. Внутривенное введение гамма-глобулин используется для лечения агаммаглобулинемии и общего вариабельного иммунодефицита.
Антибиотики назначаются людям с агаммаглобулинемией при бактериальных инфекциях. Некоторых пациентов лечат антибиотиками в качестве профилактической меры (профилактически). Все люди с иммунодефицитом должны быть максимально защищены от воздействия инфекционных заболеваний. Следует по возможности избегать кортикостероидов или любых лекарств, которые подавляют иммунную систему (иммунодепрессанты), а также таких физических нагрузок, как грубые контактные виды спорта, которые могут повредить селезенку.
Хирургия
Как уже отмечалось выше, у людей с иммунодефицитом с повышенным уровнем IgM наблюдается склонность к кровотечениям, чрезмерно связанным с аномально низким уровнем циркулирующих тромбоцитов в крови (тромбоцитопения). Это может осложнить любую хирургическую процедуру.
Прогноз
Агаммаглобулинемия имеет благоприятный прогноз при условии постоянного введения гамма-глобулином и осуществления адекватной терапии антибиотиками.
Несвоевременное применение антибактериальной терапии при обострении инфекционных болезней может привести к стремительному прогрессированию патологического процесса и летальному исходу больного.
Гипогаммаглобулинемия, болезнь Брутона, аутосомная рецессивная агаммаглобулинемия швейцарского типа
Гипогаммаглобулинемия — это заболевание, возникающее в результате дефицита В-клеток (В-лимфоцитов) в сочетании с уменьшением размера антител — иммуноглобулинов. Эти антитела не только определяют чужеродные антигены, но и генерируют генетический ответ, который приводит к уничтожению этих антигенов.
Уменьшение количества антител в организме связано с периодическими инфекциями, вызываемыми конкретными формами бактерий. В случае ответа B-лимфоцитов на нарушение качества клеточного иммунитета автоматически регулируется количество бактериальных, грибковых и вирусных инфекций.
Наиболее частые разновидности нарушений, связанных с В-клетками — это непосредственно гипогаммаглобулинемия, а также агаммаглобулинемия (сцепленная с Х-хромосомой, или агаммаглобулинемия Брутона), а также аутосомная рецессивная агаммаглобулинемия швейцарского типа.
Причины, симптомы и методы лечения гипогаммаглобулинемии
В организме существует два вида лимфоцитов. Т-лимфоциты отвечают за уничтожение болезнетворных организмов, В-лимфоциты производят антитела, «налипающие» на атакующие организм патогены, таким образом, Т-лимфоциты и другие защитные клетки накапливаются и атакуют чужеродные организмы.
Антитела – это ключевые белки, ответственные за обнаружение болезнетворных патогенов, понижение их уровня увеличивает восприимчивость к инфекциям. Критическое снижение количества антител вызывает гипогаммаглобулинемию.
Причины
Гипогаммаглобулинемия может быть первичной (то есть, врожденной) или вторичной (приобретенной), вызванной заболеваниями. Первичная форма заболевания может проявиться как при рождении, так и позднее — в более старшем возрасте, несмотря на то, что дефектный ген в организме присутствует с рождения. Большинство случаев гипогаммаглобулинемии развивается после 6-месячного возраста. Случаи заболевания, проявляющиеся на 3-м или 4-м десятилетии жизни, принято считать первичным иммунодефицитом. Их развитие, полагают медики, является результатом еще не установленных генных дефектов.
Симптомы
Большинство пациентов с гипогаммаглобулинемией страдают от рецидивирующих инфекций. Острота проявления симптомов зависит от семейной истории болезни, возраста начала болезни, имеющихся в организме инфекций, состава крови, состояния ЖКТ и опорного аппарата, а также от того, имеются ли у пациента аутоиммунные заболевания или болезни сосудов.
Симптомы гипогаммаглобулинемии:
- задержка роста;
- аномалии лимфоидной ткани и органов (например, нехватка тканей миндалин, аденоиды, малый размер периферических лимфатических узлов);
- аномалии развития (например, скелета или грудной клетки);
- дефекты кожи и слизистых оболочек (рубцы, сыпь или сетчатое ливедо);
- ушные, носовые, горловые дефекты (например, перфорация барабанной перепонки, гнойные выделения из носа, сетчатая структура слизистой оболочки глотки);
- легочные нарушения (бронхоэктазы и легочный фиброз с хрипами, одышка и другие);
- сердечно-сосудистые нарушения (громкий шум в легочной артерии сердца, недостаточность трехстворчатого клапана, шум, предполагающий легочную гипертензию);
- гепатомегалия;
- отек нижних конечностей;
- неврологические нарушения (паралитический полиомиелит или глубокая потеря чувствительности со снижением вибрационных воздействий и снижением чувствительности конечностей).
Лечение
Лечение гипогаммаглобулинемии направлено на устранение основной причины недомогания, заболевание или инфекцию. Пациентам с нарушением функции Т-клеток, тяжелыми расстройствами В-клеток не назначают живые вакцины. Высокие дозы ВВИГ (внутривенного иммуноглобулина) или интератекального иммуноглобулина могут быть полезны пациентам с энтеровирусным менингоэнцефалитом. Показано применение полиэтиленгликоля при дефиците аденозиндезаминазы. Для лечения гранулематозных заболеваний применяют фактор некроза опухолей (ФНО). Успешным методом лечения является и генная терапия, наиболее эффективна она у детей с агаммаглобулинемией Брутона. У взрослых и детей старшего возраста эффективность такого метода лечения ниже.
Аутосомная рецессивная агаммаглобулинемия швейцарского типа
Тяжелый комбинированный иммунодефицит (SCID, ТКИД), или аутосомная рецессивная агаммаглобулинемия швейцарского типа, является наиболее серьезным расстройством из группы человеческих иммунодефицитов. В медицинских источниках и литературе данное заболевание известно также под названием алимфоцитоз. Это заболевание врожденного характера.
Развитие ТКИД сопровождается нарушениям работы гуморальной части иммунной системы человека. Клетки, которые должны производить иммунный ответ, не функционируют. Дети с данным заболеванием подвержены повторяющимся тяжелым инфекциям, задержке роста и ранней смерти.
ТКИД встречается у одного из пятисот тысяч новорожденных. Понятие «тяжелый комбинированный иммунодефицит» объединяет несколько заболеваний, в частности:
- агаммаглобулинемия швейцарского типа;
- дефицит аденозиндезаминазы;
- аутосомно-рецессивный тяжелый комбинированный иммунодефицит;
- синдром голых лимфоцитов;
- ТКИД с лейкопенией. У детей с этой формой заболевания отсутствуют белые клетки крови — гранулоциты.
Для того чтобы понять, почему ТКИД считается самым тяжелым расстройством среди всех типов иммунодефицитов, можно рассмотреть схему иммунной системы человека. Она состоит из трех частей: клеточной, гуморальной и неспецифической. Клеточные и гуморальные части системы необходимы для борьбы с инфекциями — они определяют возбудителей болезней и атакуют их. Клеточная система состоит из множества классов Т-лимфоцитов (белых кровяных клеток, которые обнаруживают инородных захватчиков — антигены). Гуморальная система состоит из В-клеток, которые являются единственными клетками в организме, производящими антитела. При ТКИД ни клеточная, ни гуморальная часть иммунной системы не функционирует так, как необходимо.
Причины и симптомы
SCID является наследственным заболеванием. Существует два типа неправильного развития иммунной системы плода. При первом типе генетического нарушения В- и Т-клетки являются дефектными. При втором типе только Т-клетки являются аномальными, но их недостаток влияет на функционирование лимфоцитов.
В течение первых нескольких месяцев жизни ребенок с ТКИД защищен антителами, попавшими в его организм из крови матери. Однако уже в возрасте трех месяцев ребенок с подобным нарушением начинает страдать от грибковой инфекции полости рта (молочницы), хронической диареи, отита и легочных инфекций, в том числе пневмоцистной пневмонии. Ребенок теряет вес, становится очень слабым, и, в конце концов, умирает от условно-патогенной инфекции.
Лечение аутосомной рецессивной агаммаглобулинемии
Тяжелый комбинированный иммунодефицит/агаммаглобулинемию можно лечить с помощью антибиотиков и иммунной сыворотки. Однако такие методы лечения не могут защитить больных, а лишь защищают от инфекций. Постоянная защита невозможна из-за привыкания к антибиотикам и уничтожения полезной микрофлоры ЖКТ. В настоящее время один из немногих эффективных методов лечения этого заболевания — это пересадка костного мозга.
Сцепленная с X-хромосомой агаммаглобулинемия Брутона с дефицитом гормона роста
Что такое агаммаглобулинемия Брутона?
Агаммаглобулинемия Брутона — это заболевание, относящееся к иммунодефицитам, впервые описанное в 1952 году. Огден Брутон обратил внимание на отсутствие иммуноглобулинов у мальчика с пневмонией и другими бактериальными инфекциями. Фактически именно этот тип иммунодефицита является первым официально описанным иммунодефицитом в истории медицины. Брутон был первым специалистом, обеспечившим больному специфическую иммунотерапию — с этой целью он вводил больному иммуноглобулины внутримышечно.
Состояние больного после лечения улучшилось, однако в дальнейшем, уже на четвертом десятилетии жизни, предрасположенность к болезни легких дала о себе знать.
В настоящее время данное заболевание формально называют болезнью Брутона, а фактическое название звучит как «сцепленная с Х-хромосомой агаммаглобулинемия».
Симптомы
Болезнь Брутона проявляется следующими симптомами:
- воспаление легких;
- хроническая болезнь легких;
- задержка роста;
- высокая смертность в молодом возрасте;
- наличие гемофильной палочки;
- наличие стрептококков и стафилококков;
- кашель, одышка, хрипы, шумы в сердце и легких;
- повторяющиеся заболевания горла;
- медленный набор веса;
- заболевания кожи (экзема, сыпь);
- хронический синусит;
- колит.
Лечение
Основное лечение заключается во введении в организм больных иммуноглобулина (Ig). Агрессивное лечение бактериальных инфекций антибиотиками помогает предотвратить долгосрочные осложнения. Вирусные вакцины (например, против кори, эпидемического паротита, краснухи) таким больным противопоказаны, как и членам их семей, поскольку могут вызвать развитие инфекции, связанной с этими вакцинами.
Внутривенное введение иммуноглобулина приводит к улучшению клинической картины болезни и уменьшает прогресс серьезных инфекций, таких как пневмония и менингит.
Пациенты, получающие высокие дозы ВВИГ (400-500 мг/кг каждые 3-4 недели) и у которых уровень иммуноглобулина не опускается ниже 500 мг/дл, значительно реже болеют и попадают в больницу. При бронхоэктазах доза иммуноглобулина может быть выше (до 600 мг/кг). Больные менингитом нуждаются в 1000 мг/кг иммуноглобулина из-за гематоэнцефалического барьера.
Пациентам с хроническими инфекциями заболеваний верхних и нижних дыхательных путей и последующими структурными изменениями в этих органах необходимы антибиотики широкого спектра действия. Прием антибиотиков должен сопровождаться физиотерапией грудной клетки и хирургией носовых пазух (при хроническом синусите). Основным препаратом является триметоприм-сульфаметоксазол. Допустимо использование линезолида по отношению к пенициллинорезистентным пневмококкам.
Вспомогательные препараты это: ингаляционные кортикостероиды, антилейкотриеновые препараты, бронхорасширяющие средства.
Хроническая экзема лечится увлажняющими кремами и актуальными стероидами. Рекомендуемые пищевые добавки: поливитамины и минеральные добавки. Необходимо проведение печеночных проб и, при необходимости, соответствующее лечение гепатита С и аутоиммунного гепатита, а также точное определение этиологии диареи.